Почему вода кипит в вакууме: Кипение жидкости в вакууме при разных показателях давления
Содержание
Кипение жидкости в вакууме при разных показателях давления
Всем известно, что вода закипает при температуре 100 градусов по Цельсию. Но мало кто задумывается, что такая температура кипения воды свойственна при нормальном атмосферном давлении, которое составляет 760 мм рт. ст. А ведь такой показатель, как точка кипения воды зависит от двух параметров – давления и температуры. При изменении одного фактора соответственно меняется второй.
Точка кипения воды в вакууме
Чтобы понять, какими особенностями отличается кипение воды в вакууме, для начала нужно разобраться, что это такое – процесс кипения жидкости как физическое явление. Интенсивное изменение агрегатного состояния жидкости с переходом её в пар, при определённой температуре и давлении, с формированием пузырьков по всему объёму жидкости, в молекулярной физике называют кипением.
Так как вакуум – это закрытое пространство, в котором находиться газ под давлением, значительно ниже атмосферного, температура кипения воды так же изменяется в меньшую сторону.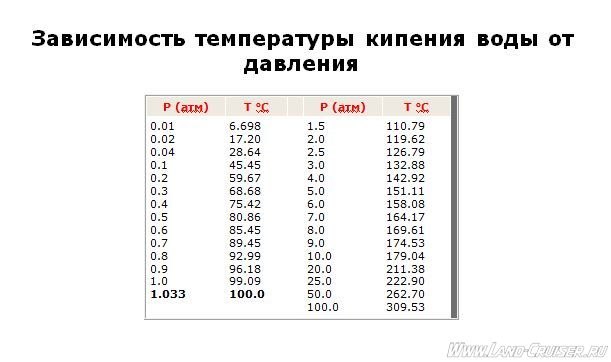 Разреженная среда способствует понижению температуры кипения. Например, понижение давления до 529 мм рт. ст. позволит закипеть воде при температуре всего 90° С. А чтобы преобразование жидкости в пар началось при комнатной температуре, необходимо в закрытом резервуаре с водой создать разряжение, например с помощью вакуумного насоса, до 20 мм рт.ст.
Разреженная среда способствует понижению температуры кипения. Например, понижение давления до 529 мм рт. ст. позволит закипеть воде при температуре всего 90° С. А чтобы преобразование жидкости в пар началось при комнатной температуре, необходимо в закрытом резервуаре с водой создать разряжение, например с помощью вакуумного насоса, до 20 мм рт.ст.
Практическое применение
На практике, такая особенность вакуума, а точнее его пониженного давления очень хорошо проверяется при подъёме в горы. На высоте 4 км над уровнем моря, атмосферное давление настолько ниже нормы, что температура кипения воды составляет всего 87° по Цельсию.
В разных отраслях промышленности, в лабораторных комплексах, в медицине и многих видах производства очень широко распространена технология вакуумной сушки. Из-за низкой точки кипения, и как результата – испарения воды, в специальных сушильных шкафах, после закладки материала, создаётся вакуум и повышается температура. Этот метод сублимированной сушки, основанный на особенностях кипения воды в вакууме, используют при пробоподготовке, проведении анализов, вулканизации, лёгком обжиге и многих других процессах, связанных с дегидратацией.
ПРИ КАКОЙ ТЕМПЕРАТУРЕ КИПИТ ВОДА?
ВАКУУМ
Онечно, при 100° по Цельсию, ответит каждый из нас. Отвечая так на этот вопрос, мы часто забываем, что наш ответ верен только для воды, находящейся под давлением воздуха на поверхности земли.
Кипение жидкости наступает тогда, когда давление пара над ней становится равным давлению воздуха или другого газа, находящегося над поверхностью жидкости. Температура кипения, следовательно,—переменная величина и зависит она от давления, под которым находится жидкость. Стоит поместить жидкость в разреженное пространство, как температура ее кипения понизится.
Поднимемся на вершину горы Казбек (5043 м выше уровня моря), где давление воздуха равно 405 мм ртутного столба, и попробуем измерить температуру «кипятка» — термометр покажет только 83°. В разреженном пространстве можно получить и совсем «холодный» кипяток. Например, при давлении в 17,5 мм ртутного столба вода будет кипеть при 20°. Это будет действительно «холодный» кипяток.
В химической, пищевой и других отраслях промышленности иногда приходится выпаривать огромные количества жидкостей. Такое выпаривание особенно эффективно в вакууме. В некоторых случаях возможность быстро выпаривать воду при низкой температуре имеет решающее значение: предохраняется от разложения растворенный продукт. При выпаривании в вакууме молока, фруктовых и ягодных соков, дрожжей, органических красителей сохраняются их важнейшие свойства.
На молочном заводе вакуум применяется не только для выпаривания молока и его сушки, но и для того, чтобы в молоко и продукты его переработки не попали загрязнения при перекачке. Чтобы из одного чана подать молоко в другой или в автоцистерну, создается вакуум и молоко само устремляется в нужном направлении.
/г баку у тому насосу Рис. 30. Установка для выпаривания в вакууме. 2 и 3 — выпарные аппараты; 4 — конденсатор для пара; 5 — трубопроводы для вторичного пара; 6 — барометрическая труба для стока конденсата. |
Используется вакуум и на консервном заводе. Чтобы убить бактерии, попавшие при упаковке в консервную банку, ее нагревают и выдерживают при повышенной температуре. Если в банке перед укупоркой останется воздух, при прогреве он расширится и может разорвать банку. Чтобы этого не случилось, перед укупоркой банку вакуумируют.
Наиболее совершенный способ сохранения продуктов в свежем состоянии состоит в быстром их замораживании и затем высушивании — вымораживании влаги под вакуумом. Это наиболее прогрессивный способ консервирования пищевых продуктов.
Можно ли создать вакуум без насоса? Да, можно. Чтобы получить вакуум без насоса, нужно часть газа путем сильного охлаждения превратить в жидкость.
Такой прием используется при выпаривании в вакууме. На рис. 30 изображена выпарная установка сахарного завода, которая состоит из нескольких, обычно трех, последовательно соединенных аппаратов. Первый из них обогревается паром, поступающим из котельной, второй — паром первого, третий — паром второго.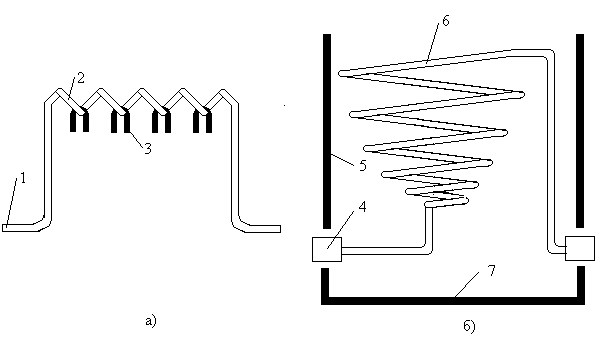 В первый аппарат поступает предварительно упаренный сироп, прошедший второй и третий аппараты. Сироп кипит, часть воды из него испаряется,
В первый аппарат поступает предварительно упаренный сироп, прошедший второй и третий аппараты. Сироп кипит, часть воды из него испаряется,
И, когда концентрация станет достаточной, сироп выпускают для кристаллизации сахара или проводят процесс кристаллизации в самом аппарате. Полученную смесь патоки и кристаллов выпускают для дальнейшей обработки. Пар из третьего аппарата поступает в конденсатор, где охлаждается водой и конденсируется. При конденсации пара создается вакуум, под которым и находится сироп в третьем корпусе выпарки. От величины вакуума зависит температура кипения сиропа в корпусах выпарки. Так как в аппараты выпарки может проникать воздух, для поддержания вакуума к конденсатору присоединен вакуум-насос. Образовавшаяся в конденсаторе вода по мере ее накопления стекает по барометрической трубке, степень заполнения которой водой определяется величиной вакуума. В каждом из выпарных аппаратов раствор кипит при пониженной температуре, так как давление в них ниже атмосферного. Это позволяет лучше использовать тепло греющего пара.
Это позволяет лучше использовать тепло греющего пара.
В химической промышленности в вакууме производится не только выпаривание, но сушка и кристаллизация многих продуктов.
В любой отрасли промышленности мы увидим использование вакуума. Многие читатели, наверное, не слышали, что даже при производстве кирпича вакуум может сыграть важную роль. В кирпичном производстве есть вид брака, который образно называется «драконов зуб». При этом кирпич выходит из пресса с рваной кромкой. Зависит это от свойств глины, и избавиться от такого вида брака трудно. И здесь помогает вакуум! Стоит создать вакуум в камере кирпичного пресса, как брак прекращается. Это происходит потому, что из глины удаляются пузырьки воздуха, глиняная масса делается более плотной и связной и лучше формуется.
Вакуум-прессы широко применяются в керамической промышленности, где требования к обработке пластичной массы особенно высоки.
металлургии также начали широко использовать вакуум, что сулит значительное повышение качества металлов. Из доменной печи выпускается огненная струя расплавленного чугуна. Заполняется огромный ковш, вмещающий десятки тонн металла, ковш подается к разливочной машине. Искры, шипение воды, шум механизмов, и вот уже бесконечная цепь тянет формы-изложницы с еще огненно — красным, но постепенно тускнеющим, застывающим чугуном. На другом конце машины из форм извлекается чугунный брусок — чушка. Та же картина у мощной мартеновской печи. Здесь сталь, сверкая всеми оттенками — от ослепительно белого и до оранжево-красного, разливается в огромные изложницы, застывает в слиток, который пойдет на мощный прокатный стан, будет обжат, вытянут, прокатан и превратится в сотни метров балок или рельсов.
Из доменной печи выпускается огненная струя расплавленного чугуна. Заполняется огромный ковш, вмещающий десятки тонн металла, ковш подается к разливочной машине. Искры, шипение воды, шум механизмов, и вот уже бесконечная цепь тянет формы-изложницы с еще огненно — красным, но постепенно тускнеющим, застывающим чугуном. На другом конце машины из форм извлекается чугунный брусок — чушка. Та же картина у мощной мартеновской печи. Здесь сталь, сверкая всеми оттенками — от ослепительно белого и до оранжево-красного, разливается в огромные изложницы, застывает в слиток, который пойдет на мощный прокатный стан, будет обжат, вытянут, прокатан и превратится в сотни метров балок или рельсов.
Но что это? После того как на получение стали затратили столько сил — плавили, разливали, охлаждали, вновь разогревали, прокатывали,— готовые рельсы отбрасывают в сторону и отправляют обратно в мартен для переплавки вместе с ржавым ломом.
Это брак! Тонкие — размером тоньше волоса — трещины, пузырьки, каверны оказались в отливке в недопустимом количестве, и готовое изделие забраковано, оно не может надежно работать.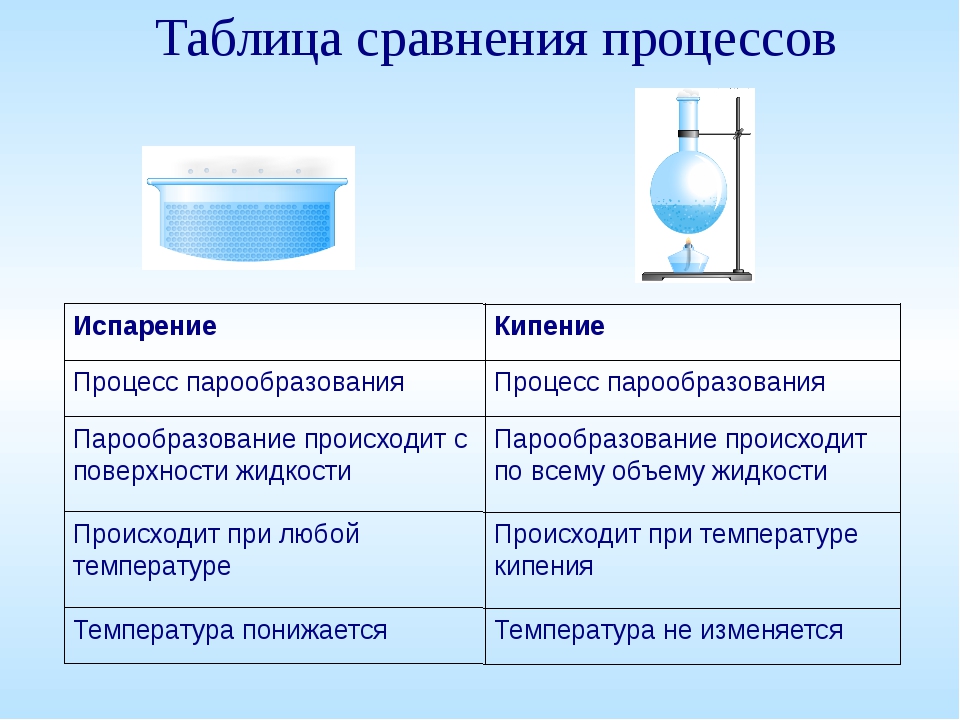
В чем дело, где причина брака? Оказывается, основной причиной самых различных пороков стали являются растворенные в металле газы. Когда металл плавят, в печи происходит ряд сложных процессов, которые в некоторых случаях сопровождаются выделением больших количеств газов. Некоторое количество газов остается в расплавленном металле. При охлаждении, когда расплавленный металл застывает в прочный и плотный слиток, газы остаются в нем, создавая дефекты. В стали могут быть растворены водород, азот, кислород. Их количество по весу невелико. Водород, например, содержится в количестве около 0,001%; но по объему это составляет 4—10 куб. см при обычном давлении на каждые 100 граммов стали. Водород заполняет небольшие пустоты в стальном слитке. В процессе охлаждения металл сжимается и в пространстве, заполненном газом, может развиться высокое давление, достигающее нескольких тысяч
Атмосфер. Такое давление образует в металле мелкие трещины — флокены. Металлурги давно борются со своим врагом — газами, растворенными в чугуне, стали и других металлах.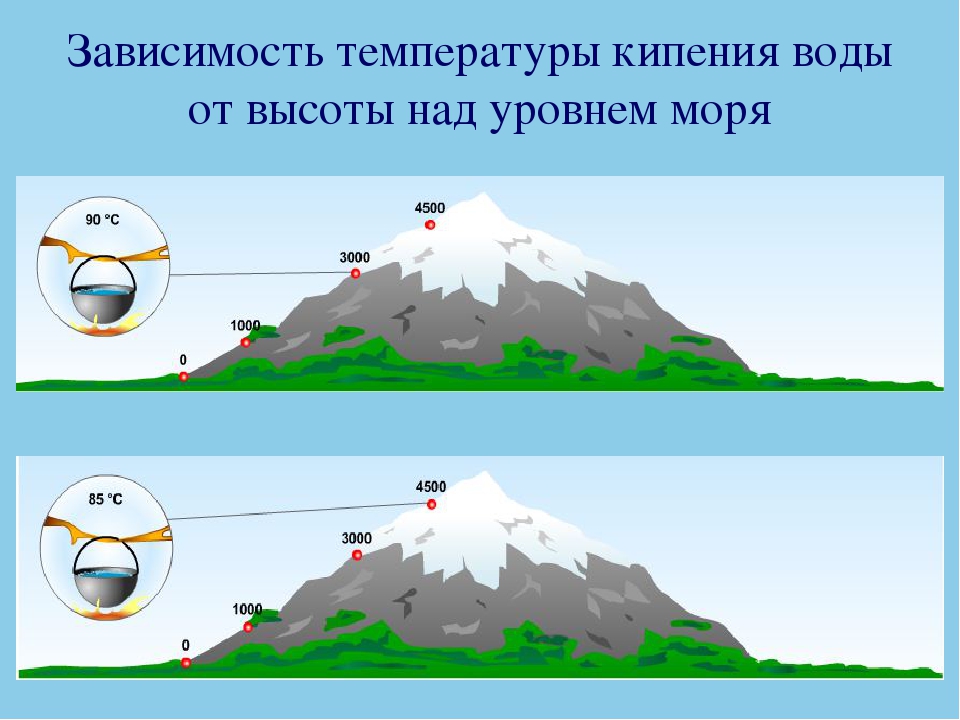 Чтобы уменьшить их количество, в металл при плавке вводятся различные вещества, которые могли бы связать газы химически. В сталь добавляют с этой целью алюминий, кремний, титан и другие вещества, но это не проходит даром. Образуются неметаллические соединения, которые понижают качество металла, даже если содержатся в сотых долях процента.
Чтобы уменьшить их количество, в металл при плавке вводятся различные вещества, которые могли бы связать газы химически. В сталь добавляют с этой целью алюминий, кремний, титан и другие вещества, но это не проходит даром. Образуются неметаллические соединения, которые понижают качество металла, даже если содержатся в сотых долях процента.
И здесь при помощи вакуума металлургам удалось повысить качество металла. Если ковш с расплавленной сталью поместить в вакуум, из нее бурно начнут выходить газы. В вакууме резко уменьшается растворимость газов в металле. Качество отливок возрастает.
Разработанные советскими учеными способы краткосрочной дегазации стали непосредственно в ковшах и изложницах уменьшают содержание в ней газов в несколько раз.
В вакууме не только удаляются примеси газов, но и во время отливки и остывания металл предохраняется от действия активных газов, прежде всего кислорода.
Высококачественные хромомолибденовые сплавы для лопаток турбин и никелевые сплавы для радиоаппаратуры плавят в вакууме, чтобы избежать окисления.
Особенно велико значение дегазации под вакуумом для специальных сталей. Подшипники из вакуумированной стали служат в три-четыре раза дольше, чем из обычной. Уменьшаются потери электроэнергии в магнитных сталях для сердечников трансформаторов. Уменьшается основной дефект жаропрочных сталей — хрупкость. Увеличивается химическая стойкость нержавеющих сталей. Одно перечисление преимуществ, которые дает применение вакуумирова — ния при плавке металлов, говорит о высокой эффективности этого процесса.
Для вакуумной плавки качественных сталей созданы индукционные печи, в которых весь процесс, включая разливку, идет в вакууме. Печь целиком помещена в герметически закрывающийся кожух, соединенный с мощными вакуум-насосами.
Большой практический интерес представляет не только плавка в вакууме, но и перегонка металлов в вакууме.
Ы ежедневно наблюдаем, как испаряются жидкости. Вы наливаете на ладонь несколько капель эфира, взмах рукой — появляется ощущение холода, и жидкость исчезает, испаряется, в воздухе распространяется запах эфира. Молекулы эфира распределились между молекулами газов воздуха.
Молекулы эфира распределились между молекулами газов воздуха.
Трудно себе представить, что подобно эфиру может испаряться сталь или другие прочные и устойчивые металлы. И действительно, сколько бы при обычной температуре мы ни держали на воздухе стальную пластинку, ее вес не уменьшится, если, конечно, воздух будет сухим и будет исключена возможность ржавления. Однако можно создать такие условия, при которых даже наиболее тугоплавкие металлы будут постепенно испаряться. Обратите внимание на старую перегоревшую электролампу. Поверхность ее стеклянного баллона изнутри покрыта темным металлическим налетом. Откуда он мог взяться? Ведь в лампе есть только нить из весьма тугоплавкого и стойкого металла вольфрама. Анализ показывает, что этот налет и состоит из вольфрама, испарившегося при накаливании нити и осевшего на холодной поверхности стеклянного баллона, совсем так же, как водяной пар, попадая на холодную поверхность, конденсируется и поверхность запотевает.
При высокой температуре металлы испаряются так же, как вода или эфир при комнатной температуре. Конечно, нужна весьма высокая температура, чтобы испарение было заметным.
Конечно, нужна весьма высокая температура, чтобы испарение было заметным.
Сравнительно легко летучими металлами являются цинк, магний, хром и некоторые другие. Так, давление пара
1 • 10″»2 мм ртутного столба достигается для цинка при 350°, магния при 439°, хрома при 917°. В то же время железо при 750° имеет давление паров только 1 • 10~8 мм ртутного столба, а вольфрам имеет такое же давление пара при температуре свыше 2100°.
Возможность испарения металлов в вакууме широко применяется в современной технике. Это свойство используется для нанесения на поверхность металлов защитных покрытий из металлического хрома. Кто из вас не любовался серебристым блеском покрытия деталей автомашин, не тускнеющих на дожде и на солнце, прочных и красивых. Это покрытие— тонкая пленка металлического хрома.
Пленка хрома может наноситься при помощи электролиза, однако использование вакуума способствовало расширению применения так называемого термохромирования. При этом способе детали и измельченный хром с определенными добавками помещаются в печь. Печь наполняют газообразным хлором, затем начинают нагрев. Хлор поглощается добавками, и в печи образуется вакуум. Хром начинает испаряться и откладываться тончайшим слоем на поверхности деталей.
Печь наполняют газообразным хлором, затем начинают нагрев. Хлор поглощается добавками, и в печи образуется вакуум. Хром начинает испаряться и откладываться тончайшим слоем на поверхности деталей.
Вакуумный метод термохромирования упрощает подготовку деталей к покрытию, сокращает расход хрома, упрощает оборудование. Когда нужен металл высокой чистоты, вакуум помогает удалить следы примесей различных веществ, например, в магнитных, жароупорных, нержавеющих сталях. Высокий вакуум необходим для удаления легколетучих примесей (свинца, кадмия, висмута) из меди.
Для получения чистых легколетучих металлов применяется плавка и дистилляция в высоком вакууме. Так же как перегоняют спирт, чтобы увеличить его крепость и отделить от примесей, перегоняют, например, ртуть, цинк, кадмий, а иногда и магний.
Даже кремнекислота, составляющая такой, казалось бы, стойкий материал, как кварцевый песок, заметно испаряется в высоком вакууме. А хром настолько летуч в высоком вакууме, что интенсивно испаряется, еще не расплавившись.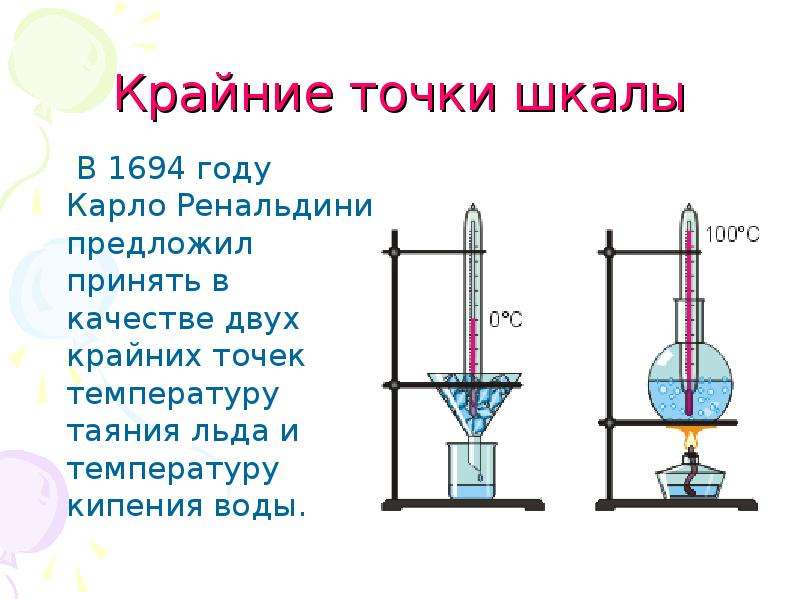
Перегонка в вакууме позволяет получить чрезвычайно чистые металлы. Удается получить алюминий, более чистый, чем при электролизе, с содержанием железа менее одной тысячной процента. Известно, что алюминий легко окисляется на воздухе, тем более активна пленка алюминия, полученная при перегонке, и только высокий вакуум предохраняет металл от окисления. Такова же роль вакуума и при плавке молибдена. Только в печи с высоким вакуумом удалось расплавить без окисления этот тугоплавкий металл, плавящийся при температуре свыше 2600° С.
Применение вакуума в металлургии привело к развитию техники получения вакуума в больших объемах и с большой скоростью. Увеличение производительности насосов позволяет размещать в вакуумируемом пространстве все более крупное оборудование.
В настоящее время уже созданы печи для единовременного расплавления 1 тонны стали при вакууме 1-10″2—
1 • 1СГ3 мм ртутного столба.
Формовка и литье под вакуумом дают весьма точные отливки.
Для применения вакуума в металлургии построены масляные диффузионные насосы с диаметром входного отверстия 80 см и скоростью откачки 14 000 л! сек, при теоретической скорости до 60 000 л! сек.
Даже беглый обзор применения вакуума в металлургии показывает, что эта важнейшая отрасль техники широко использует возможности регулировать свойства газовой среды, окружающей металл на всех этапах его «жизни» от плавки до обработки. Перспективы здесь еще более широки. Мощные вакуум-установки скоро станут такой же неотъемлемой принадлежностью металлургического завода, какой являются воздуходувные станции для подачи воздуха в печи.
М Ы познакомились с многочисленными свойствами «пустого» пространства и убедились, что оно далеко не пустое. Однако свойства многих веществ, направление ряда важных технических процессов в большой степени изменяются в разреженном …
И Спользование вакуума в повседневной жизни распространено так широко, что мы этого подчас и не замечаем. Зайдем на колхозную молочную ферму — идет доение коров. К вымени каждой из них …
Зайдем на колхозную молочную ферму — идет доение коров. К вымени каждой из них …
В Елико давление воздуха на все, находящееся на дне воздушного океана. На каждый квадратный сантиметр поверхности любого тела давит сила, равная примерно 1 кг. С тех пор как была определена …
Понижение температуры кипения в вакууме
Многие органические вещества, имеющие высокую температуру кипения и разлагающиеся при этой температуре (или несколько ниже ее), можно с успехом перегонять при уменьшенном давлении. При снижении давления до 20 мм температура кипения большинства органических веществ снижается на 100—120°. При еще более высоком вакууме наблюдается еще большее понижение температуры кипения при вакууме порядка тысячных долей миллиметра ртутного столба можно перегонять вещества, в обычном представлении являющиеся нелетучими. Зависимость между давлением и температурой кипения для некоторых веществ графически изображена на [c.35]
Благодаря понижению температуры кипения веществ в вакууме можно проводить перегонку веществ, разлагающихся при атмосферном давлении при температуре кипения. Схема установки для вакуумной перегонки приведена на рис. Е.31. Очень [c.506]
Схема установки для вакуумной перегонки приведена на рис. Е.31. Очень [c.506]
Далеко не все нефтепродукты в обычных условиях (т. е. при давлении 760 мм рт. ст.) могут кипеть без нарушения своего состава. При 360—380° и выше почти все высокомолекулярные фракции нефти (начиная с соляровой и далее) разлагаются с образованием новых соединений. Поэтому в тех случаях, когда указанное разложение нежелательно (например, при перегонке мазутов на масла), для понижения температуры кипения приходится вести перегонку при пониженном давлении, т. е. под вакуумом. Зависимость температуры кипения от давления выражается для различных жидкостей кри-.выми, аналогичными показанным на рис. Х.13. Общий характер этих кривых таков, что нри давлениях, близких к атмосферному, температура [c.163]
Во многих случаях для понижения температуры кипения раствора выпаривание ведут под вакуумом. При выпаривании под вакуумом нецелесообразно отсасывать из аппарата вакуум-насосом весь вторичный пар, так как на это расходуется много энергии. Процесс обычно ведут по схеме рис. 285. Вторичный пар поступает в конденсатор смешения или в поверхностный конденсатор (как показано на рисунке). В конденсаторе поддерживается давление, соответствующее температуре конденсации. Однако конденсирующийся пар всегда содержит некоторое количество воздуха и других неконденсирующихся газов, которые удаляют из конденсатора с помощью вакуум-насоса. [c.398]
Процесс обычно ведут по схеме рис. 285. Вторичный пар поступает в конденсатор смешения или в поверхностный конденсатор (как показано на рисунке). В конденсаторе поддерживается давление, соответствующее температуре конденсации. Однако конденсирующийся пар всегда содержит некоторое количество воздуха и других неконденсирующихся газов, которые удаляют из конденсатора с помощью вакуум-насоса. [c.398]
Перегонка в токе носителя. Понижение температуры кипения разделяемой смеси может быть достигнуто не только при перегонке под вакуумом, но также путем введения в эту смесь дополнительного компонент-носителя (водяного пара или инертного газа). [c.480]
Вследствие пониженной температуры кипения растворов потери тепла в окружающую среду, а следовательно, и расход греющего пара, идущего на компенсацию этих потерь, будут в вакуум-выпарных аппаратах значительно меньше, чем в выпарных аппаратах, работающих под атмосферным давлением. [c.408]
Ввод водяного пара в ректификационную колонну обусловлен желанием снизить температуру процесса, с тем чтобы избежать разложения нефтепродукта (перегонка мазута, тяжелых нефтяных остатков и т. п.). Температура кипения жидкости может быть снижена также понижением давления в аппарате путем создания вакуума. В нефтепереработке часто применяют оба этих способа понижения температуры кипения смеси. [c.158]
п.). Температура кипения жидкости может быть снижена также понижением давления в аппарате путем создания вакуума. В нефтепереработке часто применяют оба этих способа понижения температуры кипения смеси. [c.158]
Определим по графику понижение температуры кипения в вакууме при остаточных давлениях 100 и 5 мм рт. столба для фракции, [c.202]
Кислород из воды удаляют нагревом ее до температуры кипения, при которой растворимость кислорода (а также и других газов) снижается до нуля. Применение вакуума приводит к понижению температуры кипения. [c.130]
Простую перегонку проводят при атмосферном давлении или под вакуумом, присоединяя сборники дистиллята к источнику вакуума. Применение вакуума дает возможность разделять термически малостойкие смеси и, вследствие понижения температуры кипения раствора, использовать для обогрева куба пар более низких параметров. [c.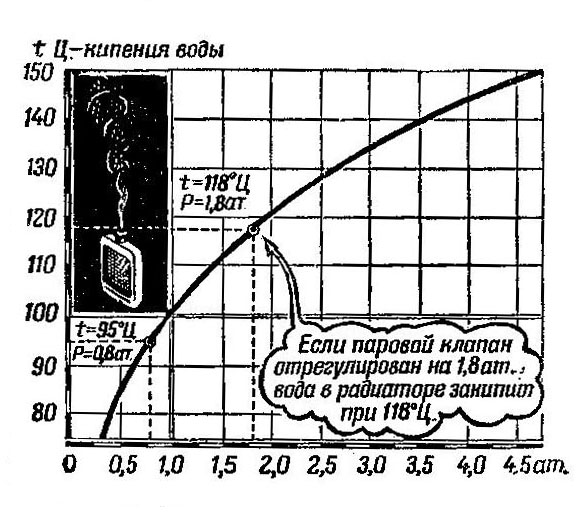 480]
480]
Понижение температуры кипенИя жидкости, достигаемое уменьшением давления, способствует сохранению химической индивидуальности перегоняемого (вещества (рис. 34). Чем выше вакуум при перегонке вещества, тем ниже температура, при которой оно будет перегоняться, и тем больше уверенности в том, что оно не будет изменяться. [c.271]
Понижение температуры кипения в вакууме имеет особое значение в области наиболее низких температур. Так, при максимальной скорости откачивания при помощи работающих на полную мощность диффузионных насосов удалось охладить жидкий гелий от т. кип. 4,22° до 0,71° К- Аналогично можно получить любую температуру вплоть до тройной точки 14° К (давление 54 мм [c.87]
Антраценовое масло, кипящее в интервале 270—340 °С. Для понижения температуры кипения часто перегоняется под вакуумом. Содержит антрацен, фенантрен, карбазол и многоядерные углеводороды. [c.435]
Для понижения температуры кипения смолы, кроме вакуума, применяют еще перегонку с перегретым водяным паром. [c.147]
[c.147]
Процессы химической технологии приходится часто осуществлять не под атмосферным или избыточным давлением, а в разреженной среде (в вакууме). Это диктуется во многих случаях условиями протекания химических реакций, необходимостью понижения температуры кипения термолабильных жидкостей, возможностью использования дешевых низкотемпературных теплоносителей и т. п. Остаточные давления Ро. используемые в химической технике, редко бывают менее, а в научных исследованиях — значительно ниже 1,35 мПа. Достигаемый вакуум принято выражать в процентах от нормального давления р , т. е. ра — Ро)/Ра 100%. [c.169]
Синтетические душистые вещества (СДВ) по химическому строению являются многофункциональными, реакционноспособными соединениями. Даже при комнатной температуре они нестойки и нуждаются в особых условиях хранения. При нагревании скорости деструкции, полимеризации (осмоления) значительно увеличиваются. По этой причине простая перегонка в производстве СДВ почти не применяется. Для понижения температуры кипения термолабильных веществ применяют вакуум. В вакууме, как и при нормальном давлении, жидкость закипает, когда упругость паров ее начинает превышать остаточное давление в аппарате. [c.296]
Для понижения температуры кипения термолабильных веществ применяют вакуум. В вакууме, как и при нормальном давлении, жидкость закипает, когда упругость паров ее начинает превышать остаточное давление в аппарате. [c.296]
Экономичность процесса ректификации достигается при использовании различных приемов понижения температуры кипения различных продуктов, например, за счет снижения давления в системе (перегонка в вакууме) и перегонки с водяным паром. [c.28]
Она представляет собой вакуумный адиабатический калориметр и криостат. Последний состоит из двух сосудов Дьюара. В наружный сосуд заливается жидкий азот, а во внутренний — жидкий гелий или жидкий азот в зависимости от требуемого охлаждения. Жидкий азот в наружном сосуде находится при атмосферном давлении, а во внутреннем создается вакуум для понижения температуры кипения сжиженного газа. [c.59]
Перегонка под вакуумом и перегонка с водяным паром применяется для разделения смесей, состоящих из труднолетучего вещества, содержащего примеси нелетучего вещества. Разделение достигается понижением температуры кипения труднолетучего компонента. [c.503]
Разделение достигается понижением температуры кипения труднолетучего компонента. [c.503]
В разреженном пространстве все жидкости кипят при более низких температурах, чем при атмосферном давлении. Это дает возможность уменьшить величину поверхности теплообмена в вакуум-выпарном аппарате, так как при пониженной температуре кипения достигается значительно большая разность температур между греющим паром и кипящим, раствором. При выпаривании в вакууме можно использовать пар низкого давления, что очень важно, когда имеется отработанный (мятый) пар. [c.398]
Указанная реакция разложения протекает частично уже при попытке подвергнуть перегонке молочную кислоту при высокой температуре. Для понижения температуры кипения кислоты эту операцию проводят только в вакууме. [c.175]
Наряду с применением вакуума, для разделения высококипящих продуктов, не растворимых в воде, применяется ректификация в токе водяного пара. Этот прием удобен при разделении смеси, отличающейся высоким значением коэффициента относительной летучести и высоким давлением паров низкокипящего компонента. Проведение ректификации такой смеси под вакуумом (для понижения температуры кипения вещества в кубе) может привести к значительным потерям низкокипящего продукта, конденсируемого при пониженном давлении. [c.489]
Проведение ректификации такой смеси под вакуумом (для понижения температуры кипения вещества в кубе) может привести к значительным потерям низкокипящего продукта, конденсируемого при пониженном давлении. [c.489]
Наконец за счет пониженной температуры кипения в вакуум-выпарных аппаратах потери тепла в окружающую среду, [c.285]
Вакуум-насосы используют в выпарных установках для понижения температуры кипения раствора, в конденсационных, фильтровальных и сушильных установках. [c.181]
В вакууме кислота (как и всякая жидкость) кипит при более низкой температуре, чем при атмосферном давлении. Из рис. 14-7 видно, что, например, 95%-ная серная кислота, кипящая под атмосферным давлением при 300 °С, под давлением 4 лш рт. ст. кипит уже при 120 °С. Такая температурная депрессия (понижение температуры кипения) позволяет сохранить большую разность температур между упариваемой кислотой и теплоносителем. Кроме того, при более низкой температуре кислота и ее пары вызывают меньшую коррозию аппаратуры. Наконец, в вакууме значительно уменьшаются потери Н ЗО . [c.384]
Кроме того, при более низкой температуре кислота и ее пары вызывают меньшую коррозию аппаратуры. Наконец, в вакууме значительно уменьшаются потери Н ЗО . [c.384]
Перегонка с паром понижает температуру кипения перегоняемой фрак . Кроме того, вызывая энергичное размешивание, она тем самым позволяет избегнуть перегрева. Понижение температуры кипения фракций возрастает с количеством вводимого пара. Когда становится необходимым затрачивать слишком большие количества пара, то более целесообразным становится применение вакуума. В этом случае жидкость начинает кипеть тогда, когда упругость ее пара делается равной противодействующему давлению очевидно, что темре-ратура кипения будет тем ниже, чем ниже давление. [c.15]
Перегонку в вакууме проводят во избежание разложения сырья из-за воздействия высоких температур. Снижение давления обеспечивает понижение температур кипения всех компонентов мазута. В результате при сравнительно низких температурах процесса перегонки, при которых еще не происходит крекинг, можно отобрать дополнительные количества дистнл-лятных фракций. Для удобства сопоставления температура кипения этих фракций пересчитывается на атмосферное давление. При вакуумной перегонке сырье целесообразно нагревать до максимально возможной допустимой температуры, чтобы достичь высокой доли отгона. Это уменьшает общий расход тепла и расход тепла в нижнюю часть колонны, где находится термически нестабильный остаток перегонки. [c.34]
Для удобства сопоставления температура кипения этих фракций пересчитывается на атмосферное давление. При вакуумной перегонке сырье целесообразно нагревать до максимально возможной допустимой температуры, чтобы достичь высокой доли отгона. Это уменьшает общий расход тепла и расход тепла в нижнюю часть колонны, где находится термически нестабильный остаток перегонки. [c.34]
Однако на первый взгляд эта идея практически неосуществима. В самом деле, Н2304 при обычных условиях кинит с разложением при 335, а этилсер-пая кислота разлагается (вне условий катализа) при 160—170 °С [11]. Следовательно, при атмосферном давлении реакция между этиленом и серной кислотой в паровой фазе невозможна. Для понижения температуры кипения,, а следовательно, и температуры паров Н28 04 можно было бы использовать вакуум но даже в вакууме вряд ли удалось бы найти условия существования моноэтилового эфира серной кислоты, так как в результате применения железа в качестве материала для реакционной аппаратуры можно ожидать понижения температуры разложения этилсерной кислоты, как и в присутствии Си, Ag, N1, когда распад этилсерной кислоты начинается уже при 100 °С. [c.28]
[c.28]
Перегонку в вакууме применяют для разделения высококипя1ЦИХ углеводородов (керосинов, смазочных масел, твердых парафинов и др.). Это вызвано необходимостью понижения температуры кипения углеводородов, чтобы избежать их разложения. Кроме того пере-гонка в шкууме применяетсйУ( кций низкокипящих углеводородов с целью увеличения относительной летучести смеси углеводородов. [c.23]
Основное преимущество выпаривания под разрежением (под вакуумом) — снижение температуры кипения раствора, что существенно для веществ, которые при более высоких температурах подвержены каким-либо нежелательным превращениям (термическое разложение, окисление, осмоление, значительное отложение твердых веществ на горячих кипятильных поверхностях и т. п.). Кроме того, понижение температуры кипения инте-сифицирует процесс передачи теплоты, так как разность температур между греющим паром и кипящим раствором при этом увеличивается. [c.310]
При нагревании охлаждающей воды происходит выделение солей и образование накипи на внешней стороне змеевиков. Очистка от накипи — операция трудоемкая и малоэффективная. Чтобы избежать накипеобразова-ния, применяют вакуумные испарители. Создание глубокого вакуума приводит к понижению температуры кипения воды до 50° С и ниже, при которой выпадения солей из воды не происходит. [c.124]
Наконец, за счет пониженной температуры кипения в вакуум- выпарных аАпаратах потери тепла в окружающую среду, а стало быть ] и расход греющего пара, идущего на компенсацию этих потерь, будут значительно меньше, чем при простом выпаривании. м [c.347]
Температура кипения воды в обычных условиях, в горах при низком давлении, вакууме
Температуру кипения необходимо знать, потому что при ее достижении вода превращается в пар, то есть переходит из одного агрегатного состояния в другое.
Мы привыкли к тому, что в кипящей воде можно дезинфицировать посуду, варить продукты, но это не всегда так. В некоторых условиях температура жидкости будет слишком низкой для всего этого.
Не забудь поделиться с друзьями!
Содержание статьи
Суть процесса
Прежде всего надо определиться с понятием кипения. Что это такое? Это процесс, при котором вещество превращается в пар. Причем процесс этот происходит не только на поверхности, но и по всему объему вещества.
При кипении начинают образовываться пузырьки, внутри которых находится воздух и насыщенный пар. Шум закипающего чайника, кастрюли указывает на то, что пузырьки воздуха начали всплывать, затем опускаться и лопаться. Когда емкость хорошо прогреется со всех сторон, шум прекратится, значит, жидкость полностью закипела.
Процесс проходит при определенной температуре и давлении и является с точки зрения физики фазовым переходом первого рода.
Обратите внимание! Испарение может происходить при любой температуре, кипение же – при строго определенной.
В таблицах температура кипения воды или другой жидкости при нормальном атмосферном давлении приводится как одна из основных физических характеристик. Температура кипения (Тк) на самом деле равняется температуре пара, который находится в насыщенном состоянии прямо на границе между водой и воздухом. Сама вода, если быть точным, нагрета чуть-чуть больше.
На процесс кипения также ощутимо влияют:
- наличие в воде примесей газа;
- звуковые волны;
- ионизация.
Есть и другие факторы, заставляющие образовываться пузырьки быстрее или медленнее. Следует также отметить, что у каждых веществ своя Тк. Бытует мнение, что если добавить в воду соль, то она закипит быстрее. Это действительно так, но время изменится совсем немного. Для ощутимых результатов придется добавить очень много соли, что полностью испортит блюдо.
Различные условия
При нормальном атмосферном давлении (760 мм рт. ст., или 101 кПа, 1 атм.) вода начинает кипеть, нагревшись до 100 ℃. Это знают все.
Важно! Если внешнее давление увеличивать, то температура кипения тоже возрастет, а если уменьшать, то станет меньше.
Уравнение зависимости температуры кипения воды от давления довольно сложное. Зависимость эта не линейная. Иногда пользуются барометрической формулой для расчета, делая некоторые приближения, и уравнением Клапейрона-Клаузиуса.
Удобнее воспользоваться таблицами из справочников, в которых приведены данные, полученные экспериментальным путем. По ним можно построить график и, проведя экстраполяцию, вычислить требуемое значение.
В горах вода закипит, не успев нагреться до 100 ℃. На самой высокой вершине мира Джомолунгме (Эверест, высота над уровнем моря 8848 м) температура закипания воды равняется приблизительно 69 ℃. Но даже если опуститься немного ниже, то все равно вода будет кипеть не при ста градусах, пока мы не достигнем давления в 101 к Па. На Эльбрусе, который ниже Эвереста, чайник с водой закипит при 82 ℃ – там давление равно 0,5 атм.
Поэтому в горных условиях для приготовления пищи потребуется значительно больше времени, а некоторые продукты вообще не сварятся в воде, их придется готовить другим способом. Иногда неопытные туристы удивляются, почему яйца так долго варятся, а кипяток не обжигает. Все дело в том, что этот кипяток недостаточно нагрет.
В автоклавах и скороварках, наоборот, давление увеличивают. Это заставляет воду кипеть при более высокой температуре. Пища сильнее разогревается, и готовка происходит быстрее. Поэтому скороварки так и назвали. Нагрев до высокой температуры полезен еще и тем, что происходит дезинфекция жидкости, в ней погибают микробы.
Кипение при повышенном давлении
Повышение давления приведет к увеличению Тк воды. При 15 атмосферах кипение начнется только при 200 градусах, при 80 атм. – 300 градусов. В дальнейшем рост температуры будет очень медленным. Максимальное значение стремится к 374,15 ℃, что соответствует 218,4 атмосферам.
Кипение в вакууме
Что будет, если воздух начнет все более и более разряжаться, стремясь к вакууму? Понятно, что температура кипения тоже начнет уменьшаться. И когда же сможет закипеть вода?
Если понизить давление до 10–15 мм рт. ст. (в 50–70 раз), то температура кипения уменьшится до 10–15 ℃. Такой водой можно охладиться.
При дальнейшем снижении давления Тк будет уменьшаться и может достигнуть температуры замерзания. В этом случае в жидком состоянии вода просто не сможет существовать. Она будет переходить изо льда сразу в газ. Это случится примерно при 4,6 мм рт. ст.
Достичь абсолютного вакуума невозможно, но сильно разряженную атмосферу можно получить, если откачивать из сосуда с водой воздух. В результате такого эксперимента можно увидеть, когда именно закипает жидкость.
Давление понижается не только при откачке воздуха. Оно снижается возле быстро вращающегося винта, например, корабельного. В этом случае возле его поверхности тоже начинается кипение. Такой процесс назвали кавитацией. Во многих случаях такое явление нежелательно, но иногда оно приносит пользу. Так, кавитацию используют в биомедицине, промышленности и при очистке поверхностей ультразвуком.
Опыты по физике «Кипение воды при комнатной температуре»
Кипение воды при комнатной температуре
Данный опыт позволяет увидеть кипение воды при комнатной температуре.
Оборудование и материалы
Прозрачный пластиковый шприц без иголки на 15 – 20 мл, вода и кусочек пластилина.
Выполнение опыта
Наберите воду в шприц, чтобы она заняла примерно половину его объема. Двигая поршень вверх, выдавите пузырек воздуха из шприца. Закройте отверстие шариком из пластилина. Теперь потяните с силой поршень вниз. Вода в шприце закипит!
Что происходит
Для начала вспомним, что кипением называется процесс парообразования во всем объеме жидкости. При нормальном атмосферном давлении (примерно 100 тысяч паскаль) вода закипает при 1000 С. При снижении давления над поверхностью воды пузырьки могут образовываться и при меньших температурах. Если давление насыщенных паров внутри пузырька больше, чем снаружи, он растет и выталкивается вверх силой Архимеда. Давление снаружи пузырька складывается из: давления воздуха на поверхность воды, давления столба жидкости и давления пленки воды, образующей пузырек. В данном опыте мы уменьшили давление воздуха на поверхность, что привело к кипению.
Проявление и использование явления в жизни
1. Глубоководное погружение
При дыхании воздухом на уровне моря в 1 мл крови содержится 0,011 мл физически растворенного азота. На глубине 40 м человек дышит воздухом, давление которого в пять раз превышает атмосферное, значит в 1 мл крови будет содержаться в 5 раз больше азота. При быстром всплытии кровь и ткани тела могут удержать только 0,011 мл в 1 мл крови. Остальное количество азота переходит из раствора в газообразное состояние. Пузырьки азота в крови могут закупорить мелкие сосуды тканей организма. Это состояние называется газовая эмболия. В зависимости от локализации газовой эмболии (сосуды кожи, мышц, центральной нервной системы, сердца и др.) у человека возникают различные расстройства (боли в суставах и мышцах, потеря сознания), которые в целом называются «кессонной болезнью».
Чтобы спасти человека от гибели его надо немедленно поместить в барокамеру, давление в которой делают таким же, как на глубине. Пузырьки азота растворяются, и человек чувствует себя лучше. Затем медленно понижают давление (декомпрессия), чтобы «лишний» азот успел выйти из крови путем естественного газообмена через легкие.
2. Скороварка
Чтобы приготовить быстрее некоторые продукты, например мясо, используют скороварку. Это устройство внешне напоминает кастрюлю, только крышка в ней прикручивается. Вода в таких устройствах кипит при 1100 С, так как давление паров внутри больше атмосферного. Такой метод приготовления ускоряет сам процесс, сохраняет многие химические и органические соединения полезные для организма, а также убивает большее количество микробов, которые содержатся в пище.
Вопросы:
1. Почему мясо не варят в обычных кастрюлях в горах?
2. Почему подъем аквалангиста с глубины 40 м длится не менее часа?
3. Почему пузырьки образуются, прежде всего на стенках шприца?
Зависимость температуры кипения от давления. Движение. Теплота
Зависимость температуры кипения от давления
Температура кипения воды равна 100 °C; можно подумать, что это неотъемлемое свойство воды, что вода, где бы и в каких условиях она ни находилась, всегда будет кипеть при 100 °C.
Но это не так, и об этом прекрасно осведомлены жители высокогорных селений.
Вблизи вершины Эльбруса имеется домик для туристов и научная станция. Новички иногда удивляются, «как трудно сварить яйцо в кипятке» или «почему кипяток не обжигает». В этих случаях им указывают, что вода кипит на вершине Эльбруса уже при 82 °C.
В чем же тут дело? Какой физический фактор вмешивается в явление кипения? Какое значение имеет высота над уровнем моря?
Этим физическим фактором является давление, действующее на поверхность жидкости. Не нужно забираться на вершину горы, чтобы проверить справедливость сказанного.
Помещая подогреваемую воду под колокол и накачивая или выкачивая оттуда воздух, можно убедиться, что температура кипения растет при возрастании давления и падает при его уменьшении.
Вода кипит при 100 °C только при определенном давлении – 760 мм Hg.
Кривая температуры кипения в зависимости от давления показана на рис. 98. На вершине Эльбруса давление равно 0,5 атм, этому давлению и соответствует температура кипения 82 °C.
А вот водой, кипящей при 10–15 мм Нg, можно освежиться в жаркую погоду. При этом давлении температура кипения упадет до 10–15 °C.
Можно получить даже «кипяток», имеющий температуру замерзающей воды. Для этого придется снизить давление до 4,6 мм Hg.
Интересную картину можно наблюдать, если поместить открытый сосуд с водой под колокол и откачивать воздух. Откачка заставит воду закипеть, но кипение требует тепла. Взять его неоткуда, и воде придется отдать свою энергию. Температура кипящей воды начнет падать, но так как откачка продолжается, то падает и давление. Поэтому кипение не прекратится, вода будет продолжать охлаждаться и в конце концов замерзнет.
Такое кипение холодной воды происходит не только при откачке воздуха. Например, при вращении гребного корабельного винта давление в быстро движущемся около металлической поверхности слое воды сильно падает и вода в этом слое закипает, т.е. в ней появляются многочисленные наполненные паром пузырьки. Это явление называется кавитацией (от латинского слова cavitas – полость).
Снижая давление, мы понижаем температуру кипения. А увеличивая его? График, подобный нашему, отвечает на этот вопрос. Давление в 15 атм может задержать кипение воды, оно начнется только при 200 °C, а давление в 80 атм заставит воду закипеть лишь при 300 °C.
Итак, определенному внешнему давлению соответствует определенная температура кипения. Но это утверждение можно и «перевернуть», сказав так: каждой температуре кипения воды соответствует свое определенное давление. Это давление называется упругостью пара.
Кривая, изображающая температуру кипения в зависимости от давления, является одновременно и кривой упругости пара в зависимости от температуры.
Цифры, нанесенные на график температуры кипения (или на график упругости пара), показывают, что упругость пара меняется очень резко с изменением температуры. При 0 °C (т.е. 273 K) упругость пара равна 4,6 мм Hg, при 100 °C (373 K) она равна 760 мм, т. е, возрастает в 165 раз. При повышении температуры вдвое (от 0 °C, т.е. 273 K, до 273 °C, т.е. 546 K) упругость пара возрастает с 4,6 мм Hg почти до 60 атм, т.е. примерно в 10000 раз.
Поэтому, напротив, температура кипения меняется с давлением довольно медленно. При изменении давления вдвое – от 0,5 атм до 1 атм, температура кипения возрастает от 82 °C (т.е. 355 K) до 100 °C (т.е. 373 K) и при изменении вдвое от 1 атм до 2 атм – от 100 °C (т.е. 373 K) до 120 °C (т.е. 393 K).
Та же кривая, которую мы сейчас рассматриваем, управляет и конденсацией (сгущением) пара в воду.
Превратить пар в воду можно либо сжатием, либо охлаждением.
Как во время кипения, так и в процессе конденсации точка не сдвинется с кривой, пока превращение пара в воду или воды в пар не закончится полностью. Это можно сформулировать еще и так: в условиях нашей кривой и только при этих условиях возможно сосуществование жидкости и пара. Если при этом не подводить и не отнимать тепла, то количества пара и жидкости в закрытом сосуде будут оставаться неизменными. Про такие пар и жидкость говорят, что они находятся в равновесии, и пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Кривая кипения и конденсации имеет, как мы видим, еще один смысл – это кривая равновесия жидкости и пара. Кривая равновесия делит поле диаграммы на две части. Влево и вверх (к большим температурам и меньшим давлениям) расположена область устойчивого состояния пара. Вправо и вниз – область устойчивого состояния жидкости.
Кривая равновесия пар – жидкость, т.е. кривая зависимости температуры кипения от давления или, что то же самое, упругости пара от температуры, примерно одинакова для всех жидкостей. В одних случаях изменение может быть несколько более резким, в других – несколько более медленным, но всегда упругость пара быстро растет с увеличением температуры.
Уже много раз мы пользовались словами «газ» и «пар». Эти два слова довольно равноправны. Можно сказать: водяной газ есть пар воды, газ кислород есть пар кислородной жидкости. Все же при пользовании этими двумя словами сложилась некоторая привычка. Так как мы привыкли к определенному относительно небольшому интервалу температур, то слово «газ» мы применяем обычно к тем веществам, упругость пара которых при обычных температурах выше атмосферного давления. Напротив, о паре мы говорим тогда, когда при комнатной температуре и давлении атмосферы вещество более устойчиво в виде жидкости.
При какой температуре кипит вода? | Вакуум
Конечно, при 100° по Цельсию, ответит каждый из нас. Отвечая так на этот вопрос, мы часто забываем, что наш ответ верен только для воды, находящейся под давлением воздуха на поверхности земли.
Кипение жидкости наступает тогда, когда давление пара над ней становится равным давлению воздуха или другого газа, находящегося над поверхностью жидкости. Температура кипения, следовательно,— переменная величина и зависит она от давления, под которым находится жидкость. Стоит поместить жидкость в разреженное пространство, как температура ее кипения понизится.
Поднимемся на вершину горы Казбек (5043 м выше уровня моря), где давление воздуха равно 405 мм ртутного столба, и попробуем измерить температуру «кипятка» — термометр покажет только 83°. В разреженном пространстве можно получить и совсем «холодный» кипяток. Например, при давлении в 17,5 мм ртутного столба вода будет кипеть при 20°. Это будет действительно «холодный» кипяток.
В химической, пищевой и других отраслях промышленности иногда приходится выпаривать огромные количества жидкостей. Такое выпаривание особенно эффективно в вакууме. В некоторых случаях возможность быстро выпаривать воду при низкой температуре имеет решающее значение: предохраняется от разложения растворенный продукт. При выпаривании в вакууме молока, фруктовых и ягодных соков, дрожжей, органических красителей сохраняются их важнейшие свойства.
На молочном заводе вакуум применяется не только для выпаривания молока и его сушки, но и для того, чтобы в молоко и продукты его переработки не попали загрязнения при перекачке. Чтобы из одного чана подать молоко в другой или в автоцистерну, создается вакуум и молоко само устремляется в нужном направлении.
Используется вакуум и на консервном заводе. Чтобы убить бактерии, попавшие при упаковке в консервную банку, ее нагревают и выдерживают при повышенной температуре. Если в банке перед укупоркой останется воздух, при прогреве он расширится и может разорвать банку. Чтобы этого не случилось, перед укупоркой банку вакуумируют.
Наиболее совершенный способ сохранения продуктов в свежем состоянии состоит в быстром их замораживании и затем высушивании — вымораживании влаги под вакуумом. Это наиболее прогрессивный способ консервирования пищевых продуктов.
Можно ли создать вакуум без насоса? Да, можно. Чтобы получить вакуум без насоса, нужно часть газа путем сильного охлаждения превратить в жидкость.
Такой прием используется при выпаривании в вакууме. На рис. 30 изображена выпарная установка сахарного завода, которая состоит из нескольких, обычно трех, последовательно соединенных аппаратов. Первый из них обогревается паром, поступающим из котельной, второй — паром первого, третий — паром второго. В первый аппарат поступает предварительно упаренный сироп, прошедший второй и третий аппараты. Сироп кипит, часть воды из него испаряется, и, когда концентрация станет достаточной, сироп выпускают для кристаллизации сахара или проводят процесс кристаллизации в самом аппарате. Полученную смесь патоки и кристаллов выпускают для дальнейшей обработки. Пар из третьего аппарата поступает в конденсатор, где охлаждается водой и конденсируется. При конденсации пара создается вакуум, под которым и находится сироп в третьем корпусе выпарки. От величины вакуума зависит температура кипения сиропа в корпусах выпарки. Так как в аппараты выпарки может проникать воздух, для поддержания вакуума к конденсатору присоединен вакуум-насос. Образовавшаяся в конденсаторе вода по мере ее накопления стекает по барометрической трубке, степень заполнения которой водой определяется величиной вакуума. В каждом из выпарных аппаратов раствор кипит при пониженной температуре, так как давление в них ниже атмосферного. Это позволяет лучше использовать тепло греющего пара.
Установка для выпаривания в вакууме…
В химической промышленности в вакууме производится не только выпаривание, но сушка и кристаллизация многих продуктов.
В любой отрасли промышленности мы увидим использование вакуума. Многие читатели, наверное, не слышали, что даже при производстве кирпича вакуум может сыграть важную роль. В кирпичном производстве есть вид брака, который образно называется «драконов зуб». При этом кирпич выходит из пресса с рваной кромкой. Зависит это от свойств глины, и избавиться от такого вида брака трудно. И здесь помогает вакуум! Стоит создать вакуум в камере кирпичного пресса, как брак прекращается. Это происходит потому, что из глины удаляются пузырьки воздуха, глиняная масса делается более плотной и связной и лучше формуется.
Вакуум-прессы широко применяются в керамической промышленности, где требования к обработке пластичной массы особенно высоки.
% PDF-1.4
%
215 0 объект
>
эндобдж
xref
215 79
0000000016 00000 н.
0000002517 00000 н.
0000002676 00000 н.
0000003328 00000 н.
0000003752 00000 н.
0000004093 00000 п.
0000004710 00000 н.
0000005271 00000 н.
0000005744 00000 н.
0000006117 00000 п.
0000006536 00000 н.
0000006872 00000 н.
0000006984 00000 н.
0000007098 00000 н.
0000007229 00000 н.
0000007643 00000 н.
0000008080 00000 н.
0000008681 00000 п.
0000009158 00000 н.
0000010110 00000 п.
0000010635 00000 п.
0000011073 00000 п.
0000011599 00000 п.
0000012713 00000 п.
0000012893 00000 п.
0000013789 00000 п.
0000013968 00000 п.
0000014146 00000 п.
0000014363 00000 п.
0000015595 00000 п.
0000016581 00000 п.
0000016763 00000 п.
0000017052 00000 п.
0000017243 00000 п.
0000017630 00000 п.
0000018124 00000 п.
0000018940 00000 п.
0000020246 00000 п.
0000021369 00000 п.
0000025936 00000 п.
0000028342 00000 п.
0000036135 00000 п.
0000042786 00000 н.
0000046364 00000 н.
0000046483 00000 п.
0000046553 00000 п.
0000046637 00000 п.
0000049458 00000 п.
0000049719 00000 п.
0000049880 00000 п.
0000049907 00000 н.
0000050207 00000 п.
0000050930 00000 н.
0000051210 00000 п.
0000051552 00000 п.
0000051640 00000 п.
0000052003 00000 п.
0000052262 00000 п.
0000052569 00000 п.
0000052926 00000 п.
0000053195 00000 п.
0000053491 00000 п.
0000054720 00000 п.
0000055020 00000 н.
0000055382 00000 п.
0000055466 00000 п.
0000057377 00000 п.
0000057703 00000 п.
0000058126 00000 п.
0000062476 00000 п.
0000062759 00000 п.
0000065343 00000 п.
0000065382 00000 п.
0000067750 00000 п.
0000067815 00000 п.
0000068803 00000 п.
0000068842 00000 п.
0000002338 00000 п.
0000001876 00000 н.
трейлер
] / Назад 104078 / XRefStm 2338 >>
startxref
0
%% EOF
293 0 объект
> поток
hb«f`XzA , Pd`h | ɀ, 4Rig0HluŅZ% ˃XD>.tSXp \ H; v1j
Точка кипения воды — при какой температуре кипит вода?
Нормальная температура кипения воды составляет 100 ° C или 212 ° F. Изменения высоты влияют на температуру кипения, потому что они влияют на атмосферное давление.
Нормальная температура кипения воды составляет 100 ° C, 212 ° F или 373,1 K. «Нормальная температура» относится к уровню моря или высоте 0 метров над уровнем моря. Но температура кипения воды меняется с высотой. Точка кипения — это более высокая температура ниже уровня моря и более низкая температура над уровнем моря.
Факторы, влияющие на точку кипения воды
Точка кипения воды — это температура, при которой давление пара жидкости равно атмосферному давлению. Причина, по которой точка кипения изменяется с увеличением высоты, заключается в изменении атмосферного давления. Эффект заметен, если сравнить температуру кипения в долине и на вершине горы. На каждые 150 м (500 футов) увеличения высоты точка кипения воды снижается примерно на половину градуса Цельсия или один градус Фаренгейта.Но даже ежедневные изменения барометрического давления влияют на точку кипения, хотя разница температур слишком мала, чтобы ее можно было заметить.
Атмосферное давление — не единственный фактор, влияющий на температуру кипения. Примеси повышают температуру кипения за счет процесса, называемого повышением точки кипения. Например, добавление соли в воду увеличивает ее температуру кипения. Хотя некоторые люди добавляют соль в кипящую воду, потому что думают, что при более высокой температуре она приготовит пищу быстрее, эффект на самом деле слишком мал, чтобы что-то изменить.
Точка кипения в Денвере, Ла-Пасе и других местах
Вода кипит при более низкой температуре в таких городах, как Денвер и Ла-Пас, но при более высокой температуре в таких местах, как Долина Смерти и Мертвое море. Если вы живете на большой высоте, еда готовится при более низкой температуре, поэтому приготовление часто занимает больше времени. Вы не можете сделать воду горячее, если кипятите ее дольше или нагревает больше. Вот почему многие рецепты включают инструкции по приготовлению на большой высоте или рекомендуют использовать скороварку.
| Местоположение | Высота | Точка кипения (° C) | Точка кипения (° F) |
| Мертвое море | -427 м (-1401 фут) | 101,4 | 214,5 |
| Долина Смерти | -86 м (-282 футов) | 100,3 | 212,5 |
| Баку, Азербайджан (нижний столичный город) | -28 м (-92 футов) ) | 100.1 | 212,2 |
| Уровень моря | 0 м (0 футов) | 100 | 212 |
| Лондон | 14 м (36 футов) | 99,96 | 211,9 |
| Денвер | 1609 м (5280 футов) | 94,7 | 202,5 |
| Ла-Пас, Боливия (самый высокий столичный город) | 3640 м (11942 футов) | 87,8 | 190,0 |
| Mt. Эверест | 8848 м (29029 футов) | 69.9 | 157,8 |
Температура кипения воды на разной высоте.
Кипячение воды при комнатной температуре
Вы можете вскипятить воду комнатной температуры, если достаточно понизить атмосферное давление. Вы можете продемонстрировать это на себе с помощью пластикового шприца. Наберите в шприц небольшой объем воды, оставив много воздуха. Теперь положите палец на открытый конец шприца, чтобы закрыть его, и как можно быстрее потяните за поршень, чтобы снизить давление.Может потребоваться пара попыток, чтобы усовершенствовать вашу технику, но вы можете увидеть, как вода закипает. Если у вас есть доступ к вакуумному насосу, более простой способ — создать вакуум в закрытом контейнере с водой.
Посмотрите, как вакуумный насос заставляет воду закипать при комнатной температуре. (кредит: Андрейдам)
Вода замерзает или кипит в космосе?
Точно так же вода сразу закипает в космическом вакууме. Затем пар немедленно кристаллизуется в лед. Если вы наблюдаете за запуском ракеты в космос, иногда можно увидеть образование льда на поверхности.Кроме того, когда космонавты выбрасывают мочу в космос, она испаряется, прежде чем образует замороженные кристаллы.
Источники
- ДеВое, Ховард (2000). Термодинамика и химия (1-е изд.). Прентис-Холл. ISBN 0-02-328741-1.
- Голдберг, Дэвид Э. (1988). 3 000 решенных задач по химии (1-е изд.). Макгроу-Хилл. Раздел 17.43. ISBN 0-07-023684-4.
- Уэст, Дж. Б. (1999). «Барометрическое давление на Mt. Эверест: новые данные и физиологическое значение. Журнал прикладной физиологии . 86 (3): 1062–6. doi: 10.1152 / jappl.1999.86.3.1062
,
Похожие сообщения
Кипящая вода в вакууме горячая?
В вакуумной камере давление может быть очень низким. Настолько слабый, что вода может закипать при комнатной температуре.
Какая температура кипения воды в вакууме?
| Температура | Дюймы рт. Ст. Вакуум | |
|---|---|---|
| F ° | C ° | |
| 212 | 100 | 0.00 |
| 205 | 96,11 | 4,92 |
| 194 | 90 | 9,23 |
Можно ли кипятить воду при комнатной температуре?
Вы можете кипятить воду комнатной температуры, не нагревая ее. Это потому, что кипение зависит от давления, а не только от температуры.
Что произойдет, если вскипятить воду в вакууме?
Молекулы воды изначально обладают кинетической энергией, но ее недостаточно, чтобы закипеть в присутствии давления воздуха.Некоторые из наиболее энергичных молекул воды уходят (испаряются), но этот процесс идет довольно медленно. Когда мы снимаем давление воздуха, наиболее энергичные молекулы воды превращаются в водяной пар.
Можно ли сделать воду горячее кипящей?
Перегретая вода — это жидкая вода под давлением при температуре от обычной точки кипения 100 ° C (212 ° F) до критической температуры 374 ° C (705 ° F). Она также известна как «докритическая вода» или «горячая вода под давлением».”
Что увеличивает температуру кипения?
Соединения, которые могут образовывать водородные связи, будут иметь более высокие температуры кипения, чем соединения, которые могут взаимодействовать только посредством лондонских дисперсионных сил. Дополнительное рассмотрение точек кипения включает давление пара и летучесть соединения. Обычно чем более летучим является соединение, тем ниже его температура кипения.
Как снизить температуру кипения воды?
Сахар, соль или другие нелетучие растворенные вещества в воде обычно повышают температуру кипения.Напротив, алкоголь — это летучие химические вещества, которые понижают температуру кипения воды. Даже большое количество растворенного в воде обычно вызывает лишь небольшие изменения температуры кипения.
Как можно вскипятить воду без электричества или газа?
Дровяная печь или камин могут быть спасением при отключении электроэнергии, и не только как общий источник тепла. Вы также можете вскипятить воду, как на костре, поставив горшок на дровяную печь или через встроенные резервуары для воды, которые есть в некоторых моделях.
Помогает ли соль воде закипать быстрее?
«Температура морской воды будет выше, чем температура чистой воды», — сказал Гиддингс. «Но у нее все еще более высокая температура кипения, и масса все равно больше, когда вы добавляете соль в тот же объем воды, поэтому это не означает, что морская вода закипает быстрее».
От чего можно довести воду до кипения при комнатной температуре?
Как вскипятить воду при комнатной температуре
- Добавьте жидкую воду комнатной температуры в вакуумную колбу, подсоединенную к вакуумному насосу.
- Добавьте промежуточную «ловушку» для сбора водяного пара до того, как он достигнет насоса.
- Включите насос, чтобы снизить давление воздуха выше жидкой воды комнатной температуры.
Почему вода в вакууме кипит при более низкой температуре и охлаждается во время кипения?
Помещение жидкости в частичный вакуум также снижает ее температуру кипения. Причина та же: удаляя часть воздуха, окружающего жидкость, вы понижаете атмосферное давление в ней.
Могут ли жидкости существовать в вакууме?
2 ответа.Никакая жидкость не может быть полностью стабильной в вакууме, поскольку все жидкости имеют некоторое ненулевое давление пара и поэтому будут испаряться с определенной скоростью. Однако некоторые жидкости имеют исключительно низкое давление пара, поэтому их можно использовать в вакууме.
Насколько горячий пар от кипящей воды?
По большей части, пар непосредственно над поверхностью кипящей воды будет иметь температуру 100 ° C или любую другую точку кипения при вашем конкретном давлении воздуха. Пар будет находиться в тепловом равновесии с жидкой водой, поэтому его температура не будет превышать ее.
Можно ли кипятить выше 100?
Жидкая вода обычно не превышает 100 градусов Цельсия, так как это ее точка кипения (при стандартных условиях). В этот момент он претерпевает фазовый переход в пар, который все еще является водой, но в газовой фазе. Пар может (и действительно) стать горячее, чем 100 градусов по Цельсию, и в результате может быть очень опасным.
Кипяток вдвойне плох?
Если у вас есть идеально чистая, дистиллированная и деионизированная вода, ничего не произойдет, если вы ее повторно кипячете.Однако обычная вода содержит растворенные газы и минералы. … Однако, если вы слишком долго кипятите воду или повторно кипятите ее, вы рискуете сконцентрировать некоторые нежелательные химические вещества, которые могут быть в вашей воде.
Что вызывает взрыв кипящей воды?
Без пузырьков вода не может отдавать накопившееся тепло, жидкость не кипит и продолжает нагреваться выше точки кипения. Если вода ударилась или сотряслась, этого достаточно, чтобы вызвать быстрое образование пузырьков, и в результате взорвется очень горячая жидкость.
Кривые давления пара | Химия для неосновных
Как быстрее всего вскипятить воду?
Как быстрее всего вскипятить воду?
Один из первых уроков кулинарии — как кипятить воду. Да, это звучит просто, но есть пара подсказок, которые могут ускорить процесс. Один совет — закройте кастрюлю крышкой. На картинке выше видно вскипание воды и выход пара в атмосферу. Если крышка находится на кастрюле, будет выкипать меньше воды, и вода закипит быстрее.Повышение давления внутри кастрюли помогает ускорить процесс кипячения.
Кривые давления пара
Точки кипения различных жидкостей можно проиллюстрировать на кривой давления паров (, рисунок ниже). Кривая давления пара представляет собой график зависимости давления пара от температуры. Чтобы найти нормальную точку кипения жидкости, проводится горизонтальная линия слева при давлении, равном стандартному давлению. При любой температуре эта линия пересекает кривую давления пара жидкости и является точкой кипения этой жидкости.
Рисунок 13.13
Кривые давления пара.
Точки кипения жидкости также коррелируют с силой межмолекулярных сил. Напомним, что диэтиловый эфир имеет слабые силы диспергирования, а это означает, что жидкость имеет высокое давление пара. Слабые силы также означают, что для закипания диэтилового эфира не требуется большого количества энергии, поэтому он имеет относительно низкую нормальную температуру кипения, равную 34,6 ° C. Вода с ее гораздо более прочными водородными связями имеет низкое давление пара и более высокую нормальную температуру кипения, составляющую 100 ° C.
Как указывалось ранее, на температуру кипения влияет внешнее давление. На больших высотах атмосферное давление ниже. При меньшем давлении на поверхность жидкости она закипает при более низкой температуре. Это также видно из кривых давления пара. Если провести горизонтальную линию при более низком давлении пара, она пересечет каждую кривую при более низкой температуре. Температура кипения воды составляет 100 ° C на уровне моря, где атмосферное давление является стандартным. В Денвере, штат Колорадо, на высоте 1600 м над уровнем моря атмосферное давление составляет около 640 мм рт. Ст., А вода кипит при температуре около 95 ° C.На вершине горы. Эверест атмосферное давление составляет около 255 мм рт.ст., а вода кипит всего при 70 ° C. С другой стороны, вода закипает при температуре выше 100 ° C, если внешнее давление выше стандартного. Скороварки не позволяют парам выходить, и давление пара увеличивается. Поскольку теперь вода закипает при температуре выше 100 ° C, пища готовится быстрее.
Рисунок 13.14
Скороварка.
Эффект пониженного давления воздуха можно продемонстрировать, поместив стакан с водой в вакуумную камеру.При достаточно низком давлении, около 20 мм рт. Ст., Вода закипит при комнатной температуре.
Основные выводы
Сводка
- Кривая давления пара представляет собой график зависимости давления пара от температуры.
- На температуру кипения влияет внешнее давление.
Упражнения
Практика
Вопросы
Используйте видео ниже, чтобы ответить на следующие вопросы:
- Для чего нужен вакуумный насос?
- Какова роль уплотнительного кольца?
- Что происходит при включении вакуумного насоса?
- Что произошло при включении вакуумного насоса?
- Какова была температура этой кипящей воды?
Упражнения
Обзор
Вопросы
- Что показывает кривая давления пара?
- Почему диэтиловый эфир имеет низкую температуру кипения?
- Какие межмолекулярные силы удерживают вместе молекулы воды?
- Почему вода закипает при более низкой температуре на большой высоте?
Глоссарий
- Кривая давления пара: График зависимости давления пара от температуры.
7-2. Испарение жидкости (испарение) | Основы | Учить
Испарение жидкости (испарение)
Пример с пивом в «7-1. Кавитация» продемонстрировал, что газообразный диоксид углерода, растворенный в пиве, диффундирует из жидкости при понижении давления.
В этом разделе давайте рассмотрим случаи, когда жидкость сама превращается в газ (испарение), а не растворенный газ, выходящий из жидкости.
Пиво — это смесь воды, спирта и углекислого газа, но для простоты объяснения мы будем использовать чистую воду.
Вода закипает при температуре 100 градусов по Цельсию. Якобы это общеизвестно, но так ли это на самом деле?
Фактически, вода закипает только при 100 ° C, когда окружающее давление составляет 1 атмосферу (= 0,1013 МПа).
Молекулы воды начинают двигаться более интенсивно при повышенных температурах. Молекулы воды связаны друг с другом, пока температура низкая, но когда температура поднимается до определенной точки, связь разрывается из-за увеличения молекулярного движения.
Кипение воды означает, что молекулы, вырвавшиеся из связи (водяной пар), преодолевают силу на поверхности жидкости и выпрыгивают.Эта температура называется точкой кипения.
В случае открытого контейнера (не герметичного / водонепроницаемого), как показано на рис. 1, сила на поверхности жидкости — это давление воздуха (атмосферное давление).
Здесь температура, при которой вода начинает кипеть, преодолевая атмосферное давление (1 атмосфера), составляет 100 ° C. В этих условиях, когда вода закипает, температура остается на уровне 100 ° C, пока вода полностью не уйдет.
Далее накрываем емкость, укупоривая ее полностью, как показано на рис.2.
Когда мы нагреваем воду в этом состоянии, в отличие от открытого контейнера, температура продолжает расти и, наконец, превышает 100 ° C. В полностью герметичном контейнере внутреннее давление газа увеличивается и давит на поверхность жидкости — это предотвращает кипение воды внутри даже при температуре до 100 ° C.
В частности, вода кипит примерно при 100 ° C при атмосферном давлении (0,1 МПа), примерно при 120 ° C при давлении 0,2 МПа и примерно при 140 ° C при давлении 0,37 МПа.
Скороварка использует этот принцип.
В скороварке можно готовить рис при температуре выше 100 ° C, создавая внутри контейнера для варки среду под высоким давлением (в пределах атмосферного давления + 0,1 МПа). В результате рис можно приготовить до совершенства за короткое время.
Давайте теперь рассмотрим обратное.
Обращаясь к примеру скороварки, мы теперь снизим давление внутри герметичного контейнера. Мы делаем это, удаляя воздух внутри контейнера с помощью вакуумного насоса. (Рисунок.3)
Предположим, мы снизили давление внутри контейнера до -0,05 МПа, как показано на рис. 4. Здесь сила давления на поверхность жидкости ослабевает, что облегчает кипение воды. Другими словами, температура кипения ниже — вода закипает при температуре ниже 100 ° C. Как и следовало ожидать, чем ниже давление, тем ниже будет температура кипения.
В частности, вода кипит примерно при 80 ° C при -0,05 МПа, примерно при 60 ° C при -0,08 МПа и примерно при 45 ° C при -0.09 МПа.
Помните принцип работы мембранного насоса?
Когда диафрагма мембранного насоса выдвигается, внутри головки насоса возникает отрицательное давление.
Тот же эффект, что и на рис. 4, происходит внутри головки диафрагменного насоса.
Например, если теплая вода с температурой 60 ° C перекачивается диафрагменным насосом, при падении давления около 0,08 МПа внутри головки насоса или в трубопроводе на стороне всасывания эта вода закипает.
Кроме того, закипание воды внутри насоса означает, что газ попадает в головку насоса, что значительно снижает эффективность диафрагменного насоса.
Как мы уже наблюдали, превращение жидкости в газ из-за падения давления (отрицательного давления) внутри головки насоса или в трубопроводе на стороне всасывания называется кавитацией .
Мы уже подробно обсуждали, как инерционное сопротивление возникает из-за пульсации диафрагменного насоса в «2-3. Пульсация: инерционное сопротивление».«Инерционное сопротивление на стороне нагнетания создает повышенное давление, но инерционное сопротивление на стороне всасывания вызывает падение давления. Поэтому, когда инерционное сопротивление на стороне всасывания становится чрезмерным, падение давления становится значительным, что приводит к более низкому кипению. точка, что способствует более легкому испарению. Это кавитация.
Таким образом, факторы, способствующие кавитации, как и в случае инерционного сопротивления:
- а)
Легче возникает при использовании более длинного всасывающего трубопровода (шланга).
- б)
Легче возникает при более узком всасывающем трубопроводе (шланге).
- в)
Происходит легче при более высокой скорости хода.
- г)
Происходит легче при более высокой высоте всасывания насоса. (Рисунок 1)
То же самое можно сказать о всасывающей стороне стандартного диафрагменного насоса или конфигурации сдвоенного плавного насоса. Однако конфигурация сдвоенного насоса с плавным потоком имеет более высокую скорость всасывания, что означает, что инерционное сопротивление от пульсации больше, чем у стандартного мембранного насоса, при условии, что объем нагнетания такой же.Другими словами, кавитация, скорее всего, возникнет, если конструкция трубопровода неадекватна в конфигурации с двойным плавным насосом.
Существуют также другие факторы, которые могут способствовать кавитации, помимо перечисленных выше от а) до d). Эти факторы связаны с природой жидкости.
- д)
Происходит легче при более высокой температуре жидкости.
- е)
Происходит легче с жидкостями, которые легко испаряются (т. Е. Летучими жидкостями или жидкостями с низкой температурой кипения).Примеры включают метанол, ацетон и другие низкомолекулярные органические растворители.
В начало страницы
5.4A: Обзор вакуумной дистилляции
- Последнее обновление
- Сохранить как PDF
- Contributor
Кипение начинается, когда давление пара жидкости или раствора равно внешнему или приложенному давлению (часто атмосферному).\ text {th} \) ed., McGraw-Hill, 1999 , Sect. 5.28.
Автор
Лиза Николс (Общественный колледж Бьютта). Organic Chemistry Laboratory Techniques находится под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License. Полный текст доступен в Интернете.
Зачем создавать вакуум? | Нормандальский муниципальный колледж
Фил Дэниэлсон
Создание вакуума стало довольно обычным и часто рутинным занятием, но его обычность не опровергает стоимости и сложности этого.Люди постоянно борются с вакуумной техникой по очень уважительной причине. Пылесосы в некоторой степени являются обязательной частью выполнения процессов и / или являются неотъемлемой частью продукта.
Каждого специалиста по вакууму в какой-то момент спрашивали, почему им нужно пройти через все эти испытания, муки и проблемы до такой степени, что они рискуют потерять свой последний шарик. «Я должен делать это, делать то, что я делаю», — может быть временно приемлемым ответом, но есть очень реальные и простые ответы.По сути, для того, чтобы что-то сделать, необходимо удалить определенное количество молекул из емкости (камеры). Если тогда вы немного разберетесь в теме; вопрос не такой уж и сложный.
Если мы примем во внимание, что создание вакуума — это не что иное, как удаление молекул газа из контейнера до тех пор, пока количество молекул в объеме не станет меньше, чем количество молекул в том же объеме вне контейнера, мы можем начать разработку ряда причин для делать это.
Эту пониженную молекулярную популяцию можно рассматривать как давление, количество молекул, расстояние между молекулами, количество столкновений молекул или количество столкновений молекул с поверхностью.Хотя все эти представления физически взаимосвязаны и взаимозависимы, любая из этих возможных причин может быть включена в описание процесса с соответствующими требованиями и обоснованиями.
И физические, и химические эффекты действуют по отдельности или в комбинации.
Физические эффекты
Физические эффекты вступают в игру, когда физические свойства газа или газов будут либо главной проблемой процесса, либо будут способствовать или замедлять процесс.
Перепад давления
Если молекулы газа удаляются из трубы или сосуда, между молекулами и поверхностью будет меньше ударов, чем снаружи сосуда, где он подвергается воздействию атмосферы. Чем меньше молекул, тем меньше будет столкновений и тем ниже будет общая сила.
Как и многие другие физические эффекты, это также можно использовать для измерения давления, используя перепад давления для приложения силы, пропорциональной давлению.Это легко демонстрируется манометром с U-образной трубкой, в котором столб жидкости уравновешивается атмосферным давлением, реагируя на перепад давления, что приводит к измеряемой высоте столба жидкости, как показано на рисунке 1.
В практическом смысле процесса этот перепад давления, возникающий в результате удаления молекул для уменьшения количества молекул, сталкивающихся с поверхностью, может использоваться для создания силы как в динамическом, так и в статическом режимах.
Динамические приложения часто используются для перемещения твердого или жидкого материала по трубе или воздуховоду, где более высокое атмосферное давление подталкивает материал к более низкому давлению в попытке уравновесить давление с обеих сторон.Примеров, где требуется движущая сила, таких как пневмотранспортная трубка, вакуумная фильтрация или даже первое метро, предостаточно. В статическом смысле перепад давления часто используется для обеспечения фиксации на месте, например, вакуумных зажимных приспособлений или прижимов. На рис. 2 показан перепад давления в фунтах на квадратный дюйм в зависимости от давления.
Теплообмен
Передача тепла при атмосферном давлении в основном осуществляется либо прямым переносом во время столкновений молекул газа с молекулами, либо конвекцией молекулярного движения.Если два объекта с разными температурами поместить в камеру при атмосферном давлении, Тепло начнет течь от более горячего к более холодному через молекулы газа; но если давление снижается за счет удаления некоторых молекул газа, расстояние между молекулами станет больше, а количество столкновений молекул станет меньше, что приведет к уменьшению теплового потока.
Понижение теплопроводности теплоносителя (молекул газа) будет означать, что более горячий объект будет стремиться сохранять свое тепло.Если давление постоянно снижается, тепловой поток также будет постоянно уменьшаться. Таким образом, вакуум между горячими и холодными объектами станет теплоизолятором, степень изоляции которого будет определяться степенью вакуума (недостатком молекул) между ними. Этот изолирующий эффект вакуума имеет ряд практических применений.
Возможно, наиболее известной является почтенная фляжка Дьюара или термос, показанная на рис. 3, которая обычно используется для поддержания тепла или холода.Это легко приводит к другим применениям, таким как транспортные линии для сжиженных газов, которые окружены кольцевой трубой с вакуумом между трубками, чтобы предотвратить попадание тепла в жидкость и ее испарение.
Как и в случае механического воздействия перепада давления, теплопроводность может использоваться в качестве метода измерения давления, когда провод нагревается путем приложения постоянной мощности, а тепловые потери провода указываются его температурой, которая измеряется напрямую (датчик термопары ) или по сопротивлению (датчик Пирани).
Те же эффекты, что и при теплопроводности, также могут быть применены к звуковой или электрической изоляции с некоторыми специфическими сложными отличиями.
Испарение
Практически любой материал испарится, если он достаточно горячий, но вакуумные процессы, как правило, в основном связаны с испарением жидкостей. Жидкость, которая имеет какую-либо летучесть при комнатной температуре, рано или поздно испарится при атмосферном давлении. С практической точки зрения, скорее, раньше лучше, чем позже, поэтому важны средства для увеличения скорости испарения.
Поскольку испарение — это действительно молекулы жидкости, покидающие поверхность и не возвращающиеся в виде жидкости, увеличение скорости испарения будет означать увеличение количества молекул, покидающих поверхность за заданное время.
При атмосферном давлении скорость потери будет относительно низкой из-за большого количества молекул непосредственно над поверхностью. Это означает, что испаряющаяся молекула, вероятно, немедленно столкнется с молекулой газа, потеряет свою энергию и вернется в жидкое состояние.Однако, если жидкость находится внутри камеры, из которой откачано до некоторой степени, над поверхностью будет меньше молекул. Это означает, что у испаряющейся молекулы будет меньше шансов столкнуться с молекулой газа, потому что будет меньше молекул, чтобы ударить, больше пространства между молекулами и меньше молекул, ударяющихся о поверхность жидкости.
Практическим примером может служить разница в температуре кипения воды между долиной и вершиной горы. Когда жидкость закипает, она достигает критической точки, когда тепло, добавляемое к жидкости, мгновенно превращается в испарение, поэтому температура жидкости не изменяется.По мере увеличения высоты давление уменьшается, поэтому количество молекул, препятствующих испарению, уменьшается, и испаряющимся молекулам требуется меньше энергии для преодоления потерь от столкновений с молекулами окружающего газа. На рисунке 4 показана разница в температуре кипения воды на разных высотах.
Практический вакуумный процесс — это вакуумная перегонка, при которой необходимо разделить две жидкости с разным давлением пара. Течение пленки жидкой смеси в откачанный контейнер при фиксированной температуре заставит или позволит наиболее летучей жидкости испаряться при низкой температуре, потому что меньше молекул будет доступно для предотвращения испарения, чем при атмосферном давлении.
Следовательно, быстрая перегонка для практического процесса. Следует понимать, что контейнер необходимо будет динамически перекачивать, чтобы поддерживать пониженное давление, иначе вылетающие молекулы вскоре вызовут повышение давления и затем снизят скорость испарения жидкости. Примером такого процесса может быть перегонка масла для механического насоса, когда необходимо удалить летучие компоненты с высоким давлением пара, прежде чем его можно будет использовать в вакуумном насосе.
Химические эффекты
Химические эффекты вступают в игру в большинстве случаев, когда химическая реакционная способность и свойства газов либо помогают, либо замедляют процесс.Часто это касается не только конкретных газов, о которых идет речь, но и их соответствующих концентраций.
Удаление реактивных газов
Любой контейнер, камера или водопровод в какой-то момент своей истории подвергался воздействию атмосферного воздуха. Перед тем, как какие-либо из них будут использоваться для удержания или передачи чистых технологических газов, их необходимо откачать, чтобы минимизировать вредное воздействие газов внутри, прежде чем будет введен чистый газ. Если бы этого не было, это было бы похоже на заливку очищенного химического раствора в грязный стакан.Требуемая степень чистоты газа будет определять необходимый абсолютный вакуум, поскольку все остаточные газы будут рассматриваться как загрязнители.
Например, давление кислорода 10 -3 торр привело бы к уровню загрязнения 1 PPM, если бы контейнер был снова заполнен чистым газом до атмосферного давления. Эта простая концепция давления остаточного газа может вводить в заблуждение, поскольку внутренние поверхности будут покрыты десорбирующимися молекулами воды, что приведет к уровню загрязнения до 10 частей на миллион, как только поверхность уравновесится с чистым газом.Следовательно, общее количество молекул в контейнере будет главной проблемой при таком типе эффекта.
Практическое применение, чтобы проиллюстрировать этот эффект, было бы почтенной лампой накаливания, которую нужно откачать перед засыпкой инертным газом. Любой водяной пар или кислород, оставшиеся в корпусе колбы до засыпки, становятся химически активными загрязнителями, которые вступают в реакцию с горячей вольфрамовой нитью во время работы и вызывают преждевременное выгорание.
Защита
Поскольку многие материалы подвергаются химическим реакциям с воздухом, возникает необходимость удаления молекул вблизи обрабатываемой поверхности.Единственный разумный способ сделать это — поместить материал в камеру и использовать атмосферу или ее отсутствие для защиты материала от химической реакции. В этом случае количество молекул химически активного газа, ударяющихся о поверхность, будет иметь первостепенное значение.
В некоторых процессах вакуумирование камеры осуществляется с использованием тех же соображений, которые обсуждались выше, в том смысле, что после вакуумирования камера будет снова заполнена инертным газом, чтобы удалить столько молекул химически активного газа, сколько требует процесс.В других случаях весь процесс будет происходить в вакууме, чтобы защитить материал от химической реакции.
Металлургические процессы являются яркими примерами, когда печь может быть откачана и затем заполнена инертным газом или водородом (восстановительная атмосфера), или весь термический процесс может быть проведен в то время как камера находилась в условиях динамической откачки. Фактически, такие процессы, как вакуумная пайка, часто представляют собой комбинацию, в которой печь после первоначального вакуумирования предварительно нагревается при заполнении давлением водорода, и непосредственно перед достижением температуры пайки камера вакуумируется, а затем создается всплеск температуры. до температуры текучести припоя.
Комбинированное физико-химическое воздействие
Тонкопленочные процессы являются яркими примерами тех процессов, которые требуют сочетания физических и химических воздействий. Рассмотрим простой пример нитевидного испарения алюминия на подложку, показанный на рис. 5. Скрученная вольфрамовая нить накаливания нагревается непосредственно сильным током до тех пор, пока алюминиевая скоба не расплавится и не смочит нить. Если молекулярная концентрация химически активных газов слишком высока, нить окисляется и сгорает.Кроме того, горячий алюминий окисляется. В этом случае первоочередное внимание уделяется количеству ударов молекул активного газа о поверхность. Хотя нагрев можно проводить в атмосфере инертного газа, это только часть полного набора требований к параметрам процесса.
Поскольку идея заключается в испарении молекул алюминия на подложку, испаренный алюминий должен иметь возможность достигать подложки.
Если бы количество молекул между испаряющимся алюминием и подложкой было слишком большим, столкновения молекул алюминия с газом были бы настолько высокими, что алюминий, вероятно, не смог бы достичь подложки из-за потерь энергии из-за столкновений.Кроме того, немного более низкая концентрация молекул газа может легко вызвать такой разброс в концентрации испаряющегося алюминия, что пленка на подложке не будет иметь приемлемой однородности.

