Вода кипит при: При какой температуре закипает вода
Содержание
Почему в горах вода закипает быстрее?
Вода, нагретая на уровне моря до 100°С (212°F), начинает кипеть. Это означает, что внутри объема жидкости происходит образование пузырьков водяного пара и подъем их к поверхности. Вода закипает, потому что при данной температуре давление насыщения водяного пара слегка превышает атмосферное давление.
На больших высотах над уровнем моря атмосферное давление существенно уменьшается и вода кипит при более низких температурах. И наоборот, если давление над жидкостью увеличивается, например, когда вода находится ниже уровня моря или в скороварке, кипение происходит при более высокой температуре. Иллюстрация под текстом показывает температуры кипения на различных высотах над уровнем моря.
Фактор тепла и высоты
Ближний график справа показывает взаимосвязь между давлением насыщенного пара и температурой. При высоких температурах давление насыщенного пара быстро растет. Вода закипает, когда давление насыщенного пара начинает слегка превышать атмосферное давление. Именно поэтому при падении атмосферного давления уменьшается и температура кипения. На дальнем графике справа приведена зависимость температуры кипения воды от высоты над уровнем моря. Чем больше высота, тем ниже температура, при которой вода начинает кипеть.
Именно поэтому при падении атмосферного давления уменьшается и температура кипения. На дальнем графике справа приведена зависимость температуры кипения воды от высоты над уровнем моря. Чем больше высота, тем ниже температура, при которой вода начинает кипеть.
Кинетическая энергия
В процессе перехода воды в газообразное состояние важную роль играет кинетическая энергия (энергия движения) молекул. Когда энергетический уровень высок, многие молекулы испаряются, разрывая связи, удерживающие их в жидком состоянии. При низком давлении (верхний рисунок под текстом) молекулы приобретают достаточно энергии для формирования газовых пузырьков кипения без добавления большого количества тепла. Ближе к уровню моря необходимо больше тепла (красная стрелка на нижнем рисунке под текстом), чтобы парообразование имело место.
Уменьшение времени приготовления пищи
В скороварках, как, например, той, что показана на рисунке справа, создается постоянное повышенное давление. На уровне моря эти герметичные кастрюли увеличивают температуру кипения воды до 121 °С (250°F). Более высокая температура кипения означает, что продукты будут готовиться быстрее, экономя время.
На уровне моря эти герметичные кастрюли увеличивают температуру кипения воды до 121 °С (250°F). Более высокая температура кипения означает, что продукты будут готовиться быстрее, экономя время.
На продольных разрезах вверху показаны механизмы скороварки, предупреждающие чрезмерное повышение давления. Все они — предохранительный клапан (левый рисунок), регулятор давления (средний рисунок) и уплотнение ободка (правый рисунок) — помогают контролировать давление путем выпуска пара в атмосферу.
Вода кипит быстрее при закрытой крышке?
Да, вода делает котел заметно быстрее при включенной крышке.
Причина проста: для кипячения вода должна быть нагрета до точки кипения (хорошо, это было очевидно). Тем не менее, в то время как тепло подается на дно емкости, тепло также теряется на верхней части емкости с помощью трех средств: испарительного охлаждения и воздушной конвекции тепла от поверхности воды и излучения от поверхность (это последнее, вероятно, наименее значимо).
Это все равно, что выходить на улицу без шапки — вам нужно больше работать, чтобы согреться, потому что вы теряете тепло быстрее. Точно так же пламя должно вводить энергию, чтобы восполнить охлаждение в верхней части горшка.
С крышкой на кастрюле конвективное охлаждение будет существенно сокращено, так как холодный воздух не сможет циркулировать непосредственно на поверхности воды, чтобы охладить ее; Радиационное охлаждение будет немного уменьшено, потому что тепло должно будет излучаться или конвекцией к крышке, чтобы затем излучаться оттуда.
Кроме того, с крышкой на горшке испаренная вода не может диффундировать или попадать в помещение. Вскоре он достигнет равновесия давления пара и начнет конденсироваться почти так же быстро, как испаряется, возвращая большую часть скрытой теплоты испарения почти так же быстро, как теряется (это не полное восстановление, потому что емкость с крышкой не герметична ).
Таким образом, самый большой из охлаждающих эффектов будет сокращен.
Шляпа как бы на горшке 🙂
Эта статья в Mind Your Decisions показывает фактические домашние экспериментальные измерения. Кипячение 16 унций воды:
Крытая кастрюля закипела быстрее за 4 минуты и 15 секунд. Непокрытой посуде потребовались дополнительные 30 секунд, чтобы кипеть при 4 минутах и 45 секундах.
Вам придется решить, имеет ли значение разница во времени для вас. Это, безусловно, сократит ваш счет за электричество или газ на небольшое количество.
Именно уменьшенное охлаждение — по существу — теплоизоляция, как шляпа, является истинным эффектом крышки.
Кипение воды при комнатной температуре
Описание:
Кипение — процесс интенсивного парообразования, проходящий при определённой температуре — температуре кипения.
Все мы прекрасно знаем, что вода закипает при температуре 100˚С. Почему же жидкости закипают?
Почему же жидкости закипают?
Всё дело в микропузырьках газа, которые находятся внутри жидкости. В ходе нагревания внутри этих пузырьков начинает накапливаться пар. С увеличением температуры количество пара внутри пузырьков растёт и пузырьки начинают увеличиваться.
В момент, когда давление внутри пузырька сравнивается с наружным давлением, пузырёк отрывается от стенки сосуда и поднимается вверх. На поверхности жидкости он лопается и выпускает накопленный пар во внешнюю среду (при этом выпущенный пар «уносит» с собой часть энергии, тем самым охлаждая жидкость). Таким образом кипение при постоянном давлении может происходить только при определённой температуре.
Если же мы увеличим интенсивность нагрева жидкости, то количество пузырьков увеличиться и кипение будет протекать более интенсивно, а значит пар будет «уносить» ещё большее количество энергии, тем самым мешая дальнейшему повышению температуры жидкости. В таком равновесном состоянии жидкость будет находиться вплоть до полного её выкипания.
Если простыми словами, то: как бы вы не увеличивали огонь под кастрюлей с водой (хоть пионерский костер под ней разложите), температура воды в кастрюле не увеличится, если она уже закипела. Эта температура (температура кипения) будет оставаться постоянной, а увеличится только скорость кипения.
А можно ли изменить температуру кипения?
Можно! Температура кипения напрямую зависит от внешнего давления. При понижении давления время насыщения пузырьков паром уменьшиться (потому что им нужно «накачаться» до меньшего давления), а это значит, что пузырьки начнут всплывать активнее и кипение будет происходить при более низкой температуре!
Как же вскипятить воду при комнатной температуре? Очень просто! Для этого нужно лишь понизить внешнее давление до 0,04 атмосферного. Жаль только, что чай в таком кипятке завариться не сможет.
С подобной проблемой сталкиваются альпинисты: на высоте 2 километров над уровнем моря, вода начинает закипать при температуре 95 ˚С, а на высоте 5 километров при температуре 83 ˚С. В таком кипятке приготовление пищи значительно затягивается, а варка некоторых продуктов становится в принципе невозможной. (еда приготавливается из-за высокой температуры, а не от кипения)
В таком кипятке приготовление пищи значительно затягивается, а варка некоторых продуктов становится в принципе невозможной. (еда приготавливается из-за высокой температуры, а не от кипения)
Объяснение опыта:
В данном случае, с помощью специального насоса, из склянки с водой откачивается воздух. При этом давление внутри склянки падает. Чем ниже давление – тем заметнее становятся пузырьки внутри жидкости. Когда же давление уменьшается примерно до 0,04 атмосферного – жидкости внутри склянки закипает.
Это интересно:
А вы знали, что скороварки также работают благодаря связи температуры кипения жидкости с внешним давлением? В отличие от нашего опыта, в скороварках используется обратный принцип работы: давление внутри скороварки умышленно повышается, что приводит к увеличению температуры кипения. Таким образом пища готовиться гораздо быстрее, нежели при использовании привычных нам кастрюль.
Закипятить воду при комнатной температуре может каждый из вас в домашних условиях. Для этого достаточно налить в медицинский шприц немного воды и, заткнув пальцем выходное отверстие, оттянуть поршень. Давление в шприце понизится и образуются пузырьки по всему объему жидкости – вода закипела.
Для этого достаточно налить в медицинский шприц немного воды и, заткнув пальцем выходное отверстие, оттянуть поршень. Давление в шприце понизится и образуются пузырьки по всему объему жидкости – вода закипела.
Кипение — урок. Физика, 8 класс.
Вы уже изучили такой вид парообразования как испарение.
Рассмотрим второй способ образования пара — кипение.
Кипение — это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и по всему объёму.
Рассмотрим пример — кипение воды.
В воде растворены молекулы воздуха (газов). При нагревании этот растворённый газ выделяется в виде воздушных пузырьков на дне и стенках сосуда (рис. 1).
Рис. 1. Изображение кипения
С повышением температуры жидкости внутри этих пузырьков испаряется вода, они увеличиваются в размерах. Достигнув определённого размера, пузырьки отрываются от поверхности.
Если вода прогрета недостаточно, то пузырьки пара в холодных слоях схлопываются. А если температура достаточная, то они достигают поверхности воздуха или жидкости и лопаются, выпуская пар. В этот момент слышен шум, предшествующий обычно кипению. При определённой температуре вода закипает (рис. 2).
А если температура достаточная, то они достигают поверхности воздуха или жидкости и лопаются, выпуская пар. В этот момент слышен шум, предшествующий обычно кипению. При определённой температуре вода закипает (рис. 2).
Рис. 2. Изображение модели кипения
Температуру, при которой жидкость кипит, называют температурой кипения.
Обрати внимание!
Во время кипения температура жидкости не изменяется, так как вся энергия расходуется на парообразование.
Температура кипения жидкости зависит от двух факторов:
- от рода жидкости;
- от внешнего давления.
Для каждого вещества существует своя температура кипения.
| Вещество | Температура кипения (при норм. атм. давлении), °С |
| воздух | \(-193\) |
| кислород | \(-183\) |
| эфир | \(35\) |
| спирт | \(78\) |
| вода | \(100\) |
| ртуть | \(357\) |
| свинец | \(1740\) |
| медь | \(2567\) |
При уменьшении давления воздушным пузырькам легче всплывать, кипение происходит при меньшей температуре. Именно поэтому высоко в горах (на высотах \(6000\) — \(8000\) м) не варят суп или мясо, а пользуются готовыми консервами, т.к. температура кипения воды меньше \(100\)°С.
Различные жидкости одной и той же массы требуют разное количество теплоты для их обращения в пар при температуре кипения.
Q=L
·m, где
\(Q\) — количество теплоты, необходимое для обращения вещества в пар;
\(m\) — масса вещества;
\(L\) — удельная теплота.
Удельная теплота парообразования (L) — физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без ения температуры.
Источники:
Рис. 1. Автор: Monoklon — собственная работа, CC BY 4.0, https://commons.wikimedia.org/w/index.php?curid=97966488.
Все самое интересное о температуре закипания воды
Кипение – процесс перехода вещества из жидкого в газообразное состояние (парообразование в жидкости). Кипение не является испарением: оно отличается тем, что может происходить только при определенном давлении и температуре.
Кипячение – нагревание воды до температуры кипения.
[содержание]
Содержание статьи
Как происходит процесс кипения воды?
Кипение воды является сложным процессом, который происходит в четыре стадии. Рассмотрим пример кипения воды в открытом стеклянном сосуде.
На первой стадии кипения воды на дне сосуда появляются небольшие пузырьки воздуха, которые также можно заметить и на поверхности воды по бокам.
Эти пузырьки образуются в результате расширения небольших пузырей воздуха, которые находятся в мелких трещинах сосуда.
[wpmfc_short code=»Block1″]
На второй стадии наблюдается увеличение объема пузырьков: все больше пузырьков воздуха рвется на поверхность. Внутри пузырьков находится насыщенный пар.
Как только повышается температура, возрастает давление насыщенных пузырьков, в результате чего они увеличиваются в размере. Как следствие, повышается действующая на пузыри архимедова сила.
Именно благодаря этой силе пузырьки стремятся к поверхности воды. Если верхний слой воды не успел прогреться до 100 градусов С (а это и есть температура кипения чистой воды без примесей), то пузырьки опускаются вниз в более горячие слои, после чего они снова устремляются назад на поверхность.
[note]Ввиду того, что пузыри постоянно уменьшаются и увеличиваются в размере, внутри сосуда возникают звуковые волны, которые создают характерный для кипения шум.[/note]
На третьей стадии на поверхность воды поднимается огромное количество пузырьков, что вначале вызывает небольшое помутнение воды, которая затем «бледнеет». Данный процесс продолжается недолго и имеет название «кипение белым ключом».
Данный процесс продолжается недолго и имеет название «кипение белым ключом».
Наконец, на четвертой стадии кипения вода начинает интенсивно бурлить, появляются большие лопающиеся пузыри и брызги (как правило, брызги означают, что вода сильно перекипела).
Из воды начинает образовываться водяной пар, при этом вода издает специфические звуки.
Почему «цветут» стены и «плачут» окна? Очень часто в этом виноваты строители, неправильно рассчитавшие точку росы. Читайте статью Точка росы: определение чтобы узнать, насколько это важное физическое явление, и как все-таки избавиться от излишней сырости в доме?
Какую пользу может принести талая вода для желающего похудеть? Об этом вы узнаете прямо тут, оказывается, худеть можно без особых усилий!
Температура пара при кипении воды
Пар – это газообразное состояние воды. Когда пар поступает в воздух, то он, как и другие газы, оказывает на него определенное давление.
В процессе парообразования величина температуры пара и воды будет оставаться постоянной до тех пор, пока не испарится вся вода. Такое явление объясняется тем, что вся энергия (температура) направлена на превращение воды в пар.
В данном случае образуется сухой насыщенный пар. Высокодисперсные частицы жидкой фазы в таком паре отсутствуют. Также пар может быть насыщенным влажным и перегретым.
[wpmfc_short code=»Block2″]
Насыщенный пар с содержанием взвешенных высокодисперсных частиц жидкой фазы, которые равномерно распределены по всей массе пара, называется влажным насыщенным паром.
В начале закипания воды образуется именно такой пар, который затем переходит в сухой насыщенный. Пар, температура которого больше температуры кипящей воды, а точнее перегретый пар, можно получить только с использованием специального оборудования. При этом такой пар будет близок по своим характеристикам к газу.
Температура кипения соленой воды
Температура кипения соленой воды превышает температуру кипения пресной воды. Как следствие соленая вода закипает позднее пресной. В соленой воде присутствуют ионы Na+ и Cl-, которые занимают определенную область между молекулами воды.
В соленой воде молекулы воды присоединяются к ионам соли – данные процесс имеет название «гидратация». Связь между молекулами воды значительно слабее связи, образовавшейся в процессе гидратации.
[tip]Поэтому при кипении из молекул пресной воды парообразование происходит быстрее.[/tip]
На закипание воды с растворенной солью потребуется больше энергии, в качестве которой в данном случае выступает температура.
По мере увеличения температуры молекулы в соленой воде начинаются двигаться быстрее, но при этом их становится меньше, ввиду чего они сталкиваются реже. В результате образуется меньше пара, давление которого ниже, нежели у пара пресной воды.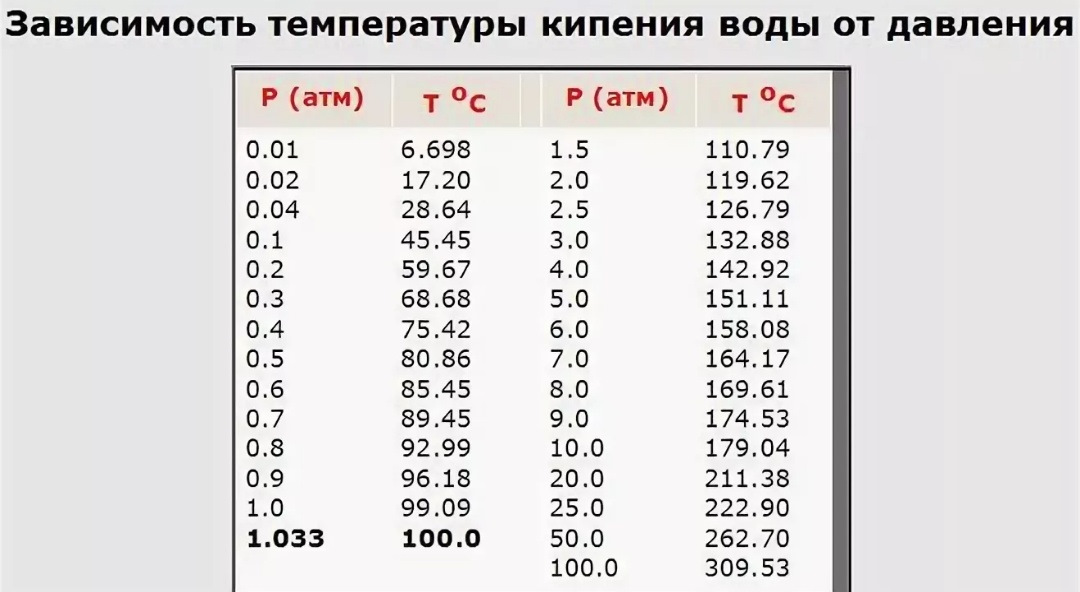
Для того чтобы в соленой воде давление стало выше атмосферного и начался процесс кипения, необходима более высокая температура. При добавлении 60 граммов соли в воду объемом 1 литр температура кипения увеличится на 10 С.
[wpmfc_short code=»Block3″]
Температура кипения воды в вакууме при различном давлении
Давление (P) — кПа | Температура (t) — °С |
10 | 45.82 |
20 | 60.07 |
30 | 69.11 |
40 | 75.88 |
50 | 81. |
60 | 85.95 |
70 | 89.96 |
80 | 93.51 |
Температура кипения воды в вакууме
Известно, что при нормальном атмосферном давлении вода закивает при температуре 100 градусах C. Нормальное атмосферное давление составляет 101,325 кПа.
При снижении окружающего давления вода закипает и испаряется быстрее. Вакуум – свободное от вещества пространство. Технический вакуум – среда, содержащая газ под давлением, которое значительно ниже атмосферного.
В вакууме остаточное давление составляет примерно 4 кПа. При таком показателе давления точкой кипения воды будет 300 С. Чем выше давление в вакууме, тем больше величина температуры кипения воды.
Температура кипения воды в чайнике
Кипяток – вода, доведенная до температуры кипения. Как правило, для получения кипятка используются чайники. Остывшая вода, прежде доведенная до кипения, называется кипяченой.
В процессе кипения воды обильно выделяется пар. Процесс парообразования сопровождается выделением из состава жидкости свободных молекул кислорода. Чистая пресная вода закипает в чайнике при температуре 100 градусов С.
В кипятке погибает большинство болезнетворных бактерий за счет длительного воздействия высокой температуры на воду. При кипении из солей, содержащихся в жесткой воде, образуется осадок, который известен нам как накипь.
Обычно кипяченую воду применяют для заваривания кофе и чая, а также для дезинфекции овощей и фруктов и т.д.
Хороший способ поправить свое здоровье — это пить минеральную воду. Узнайте больше про щелочные минеральные воды Украины названия которых наиболее известны, насколько они полезны, сколько стоят? Это интересно!
Какие сейчас цены на насосы для повышения давления воды, и как определить, стоит ли он своих денег? Об этом можно прочитать здесь, сделайте правильный выбор!
Кстати, а вы знаете, какой состав у морской воды? Об этом можно прочитать в статье:
http://pro8odu.ru/vidy-vody/seawater/pochemu-nelzya-pit-morskuyu-vodu.html, это очень интересно!
Температура кипения воды в горах
Как уже упоминалось выше, величина температуры кипения воды напрямую зависит от внешнего давления. Чем ниже будет атмосферное давление, тем меньше станет показатель температуры кипения.
Известно, что атмосферное давление значительно падает над уровнем моря. Поэтому в горах давление будет намного ниже, чем на уровне моря.
[important]Чем выше горы, тем ниже атмосферное давление, и соответственно тем ниже температура кипения воды.[/important]
Любой альпинист знает, что в горах сложно заварить чай, поскольку вода недостаточно нагревается. Также в горах требуется больше времени, чтобы сварить пищу.
Поэтому была составлена специальная таблица, отражающая температуру закипания воды в зависимости от высоты.
Температуры кипения воды на разных высотах
Высота над уровнем моря (метры) | Температура закипания воды (0С) |
0 | 100. |
500 | 98.3 |
1000 | 96.7 |
1500 | 95.0 |
2000 | 93.3 |
2500 | 91.7 |
3000 | 90.0 |
3500 | 88.3 |
4000 | 86.7 |
4500 | 85.0 |
5000 | 83. |
6000 | 80 |
Данные показатели могут меняться, если в состав воды входят примеси. При наличии нелетучих примесей температура кипения воды будет увеличиваться.
Температура кипения дистиллированной воды
Дистиллированная вода – это очищенная вода h3O, в которой практически не содержится каких-либо примесей. Обычно ее используют в медицинских, технических или исследовательских целях.
Дистиллированная вода не предназначена для питья или приготовления пищи. Такую воду производят в специальном оборудовании – дистилляторах, где происходит выпаривание пресной воды и последующая конденсация пара.
Данный процесс называется «дистилляция». После дистилляции все присутствовавшие в воде примеси остаются в выпаренном остатке.
Температура кипения дистиллированной воды будет такой же, как и у обычной водопроводной воды — 100 градусов Цельсия. Разница же заключается в том, что дистиллированная вода будет закипать быстрее по времени, нежели пресная.
Разница же заключается в том, что дистиллированная вода будет закипать быстрее по времени, нежели пресная.
Однако этот показатель практически не отличается от времени закипания обычной воды: разница состоит в считанных долях секунды.
Удельная теплота кипения воды
Удельная теплота кипения воды или парообразования – это физическая величина, отражающая количество теплоты, необходимое для превращения 1 л кипящей воды в пар.
Процесс кипения воды, как и любого другого вещества, происходит с поглощением теплоты. Значительная часть проводимой теплоты необходима для разрыва связей между молекулами воды.
Другая часть теплоты расходуется на процессы, происходящие при расширении пара. В результате поглощения теплоты увеличивается энергия взаимодействия между частицами пара.
Эта энергия становится больше энергии взаимодействия молекул воды. Таким образом, при одинаковой температуре внутренняя энергия пара становится выше внутренней энергии жидкости.
Единица удельной теплоты парообразования в системе СИ: [ L] = 1 Дж/кг.
Удельная теплота испарения воды равна 2260 кДж/кг.
Небольшое видео — измерение температуры кипения воды:
Еще интересные статьи:
Процесс кипения
☰
Если жидкость нагревать, то при определенной температуре она закипит. При кипении в жидкости образуются пузырьки, которые поднимаются наверх и лопаются. В пузырьках содержится воздух, в котором присутствует водяной пар. Когда пузырьки лопаются, то пар вырывается, и, таким образом, жидкость интенсивно испаряется.
Разные вещества, находящиеся в жидком состоянии, кипят при своей, характерной для них температуре.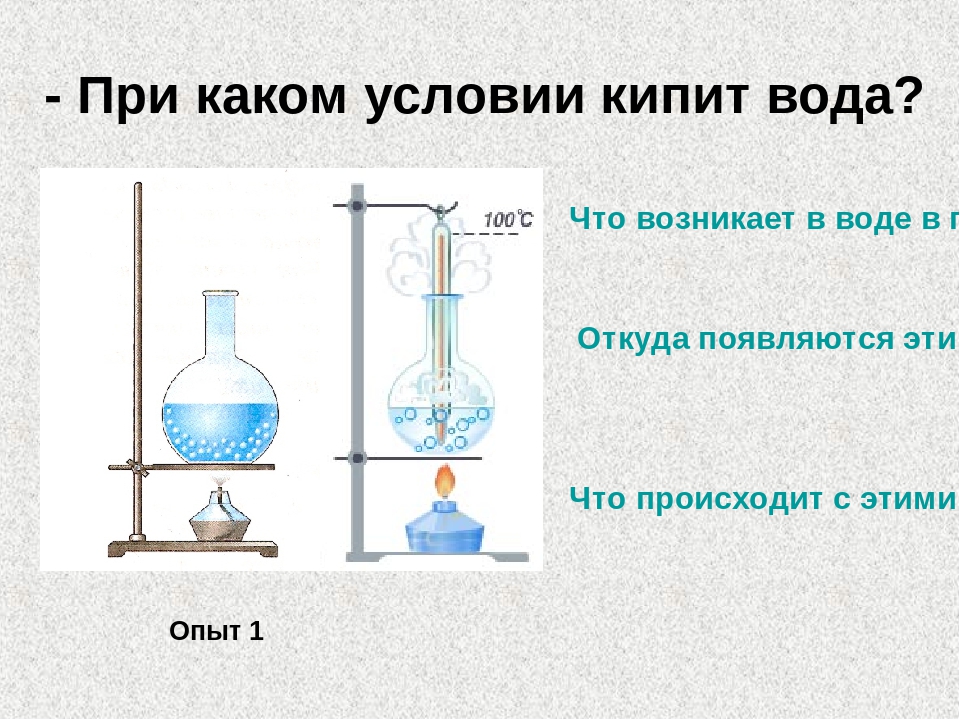 Причем эта температура зависит не только от характера вещества, но и от атмосферного давления. Так вода при нормальном атмосферном давлении кипит при 100 °C, а в горах, где давление ниже, вода кипит при более низкой температуре.
Причем эта температура зависит не только от характера вещества, но и от атмосферного давления. Так вода при нормальном атмосферном давлении кипит при 100 °C, а в горах, где давление ниже, вода кипит при более низкой температуре.
Когда жидкость закипает, то дальнейший подвод к ней энергии (тепла) не увеличивает ее температуру, а просто поддерживает кипение. То есть энергия тратится на поддержание процесса кипения, а не на поднятие температуры вещества. Поэтому в физике вводится такое понятие как удельная теплота парообразования (L). Она равна количеству тепла, необходимому для того, чтобы полностью выкипел 1 кг жидкости.
Понятно, что у различных веществ своя удельная теплота парообразования. Так у воды она равна 2,3 · 106 Дж/кг. У эфира, который кипит при 35 °C, L = 0,4 · 106 Дж/кг. У ртути, кипящей при 357 °C, L = 0,3 · 106 Дж/кг.
В чем же заключается процесс кипения? Когда вода нагревается, но еще не достигнута температура ее кипения, в ней начинают образовываться маленькие пузырьки. Обычно они образуются на дне емкости, так как обычно нагревают под дном, и там температура выше.
Обычно они образуются на дне емкости, так как обычно нагревают под дном, и там температура выше.
Пузырьки содержат воздух. Это значит, что из воды при повышении температуры выделяется растворенный в ней воздух. В пузырьки испаряется вода.
Пузырьки легче окружающей их воды и поэтому начинают подниматься в верхние слои. Однако здесь температура еще ниже, чем у дна. Поэтому пар конденсируется, пузырьки становятся меньше и тяжелее, снова опускаются вниз. Так происходит до тех пор, пока вся вода не прогреется до температуры кипения. В это время слышен шум, предшествующий кипению.
Когда достигнута температура кипения, пузырьки уже не опускаются вниз, а всплывают на поверхность и лопаются. Из них вырывается пар. В это время слышен уже не шум, а бульканье жидкости, которое говорит о том, что она закипела.
Таким образом, при кипении, также как при испарении, происходит переход жидкости в пар. Однако, в отличие от испарения, которое происходит только на поверхности жидкости, кипение сопровождается образованием пузырьков, содержащих пар, по всему объему. Также в отличие от испарения, которое происходит при любой температуре, кипение возможно лишь при определенной, характерной для данной жидкости температуре.
Также в отличие от испарения, которое происходит при любой температуре, кипение возможно лишь при определенной, характерной для данной жидкости температуре.
Почему чем выше атмосферное давление, тем температура кипения жидкости больше? Воздух давит на воду, и, следовательно, создается давление внутри воды. Когда образуются пузырьки, в них пар также давит, причем сильнее, чем внешнее давление. Чем больше давление из вне на пузырьки, тем сильнее в них должно быть внутреннее давление. Поэтому они образуются при более высокой температуре. А значит, и вода кипит при более высокой температуре.
При какой температуре кипит вода?
При какой температуре кипит вода?
Как известно, степень нагретости вещества характеризуется особой величиной — температурой.
С изменением температуры меняются многие свойства тел. При определённых температурах вещества переходят из твёрдого состояния в жидкое, из жидкого в газообразное и т. д. При повышении температуры большинство тел расширяется. Если наглухо закупорить какой-нибудь сосуд и начать его нагревать, то воздух, стремясь расшириться и не находя выхода, будет всё сильнее давить на стенки сосуда.
д. При повышении температуры большинство тел расширяется. Если наглухо закупорить какой-нибудь сосуд и начать его нагревать, то воздух, стремясь расшириться и не находя выхода, будет всё сильнее давить на стенки сосуда.
Таким образом, по изменению свойств тела можно судить о его температуре.
Но прежде нужно условиться, от какой точки и каким образом вести отсчёт температур. Ещё в XVI веке было замечено, что вода замерзает и кипит при совершенно определённых температурах. Но как обозначить эти температуры — вопрос весьма условный. Не удивительно, что долгое время разные учёные обозначали их по-разному.
Шведский учёный Андерс Цельсий (1701—1744 гг.) температуру кипения воды пометил нулём, а температуру замерзания — числом 100. Лишь впоследствии эти обозначения поменяли местами. Немецкий физик Габриель Даниель Фаренгейт (1686—1736 гг.) предложил считать, что вода кипит при температуре 212 градусов, а замерзает при тридцати двух. Нулём же он обозначил точку плавления смеси поваренной соли, нашатыря и льда. Наконец, Исаак Ньютон предложил такую температурную шкалу, в которой точка кипения воды оказалась между 33 и 34 градусами. Существовали и другие шкалы.
Наконец, Исаак Ньютон предложил такую температурную шкалу, в которой точка кипения воды оказалась между 33 и 34 градусами. Существовали и другие шкалы.
В шкале Цельсия промежуток между температурами замерзания и кипения воды разделён на 100 частей — градусов, в шкале Фаренгейта — на 180 градусов, а в шкале французского учёного Рене Антуана Реомюра (1683— 1757 гг.) — на 80. Во избежание путаницы ,после числа, означающего температуру, и знака 0 (градус) стали ставить букву, показывающую, о какой шкале идёт речь. Буква Ц означает Цельсия, Ф — Фаренгейта и Р — Реомюра.
Наибольшее распространение получила шкала Цельсия. Температуры, более низкие, чем точка замерзания воды, обозначаются в ней отрицательными числами (например,— 1°С,— 30°С и т. д.).
Существование нескольких температурных шкал мешало развитию науки и техники. Необходимо было узаконить какую-либо одну шкалу.
См. далее «измерение температуры»
FAQ: Кипение и высота / давление
Как давление влияет на кипение воды?
Почему вода закипает при более низкой температуре на больших высотах?
Все жидкости при любой температуре обладают определенным
Давление паров .
Давление пара можно представить как степень, в которой
молекулы жидкости уходят в паровую фазу.
Давление пара увеличивается с температурой, потому что при
более высокая температура молекулы движутся быстрее и больше
способен преодолевать притягивающие межмолекулярные силы, которые
имеют тенденцию связывать их вместе.Кипение происходит, когда давление пара достигает или превышает
окружающее давление из атмосферы или что-то еще в
контакт с жидкостью.
При стандартном атмосферном давлении (1 атмосфера = 0,101325 МПа),
вода закипает примерно при 100 градусах Цельсия. Это просто
другой способ сказать, что давление водяного пара при этом
температура 1 атмосфера. При более высоком давлении (например,
давление, создаваемое в скороварке), температура должна
быть выше до того, как давление пара достигнет окружающего давления,
поэтому вода под давлением закипает при более высокой температуре.По аналогии,
когда окружающее давление ниже (например, на большой высоте),
давление пара достигает этого давления при более низкой температуре.
Например, в Денвере, штат Колорадо, США.
где высота над уровнем моря
приблизительно одна миля (1600 метров), атмосферное давление
около 83% стандартной атмосферы, а вода закипает примерно при
95 градусов по Цельсию.
Связь между давлением пара и температурой (или, как выглядело
при в обратном направлении, между температурой кипения и давлением)
называется
Кривая давления паров .Кривая давления водяного пара имеет большое значение, так как она
определяет соотношение между температурой и давлением
в любом процессе, когда вода переходит из жидкости в пар
состояние или наоборот. Такие процессы важны как в
промышленность (например, парогенератор, где вода
превращается в пар в котлах и в конечном итоге конденсируется после
проходящие через турбины) и в природе (например, в
осадки и испарение из водоемов).
В следующей таблице мы указываем давление пара для воды.
в зависимости от температуры, взятой из последних
Формулировка IAPWS для общего и научного использования.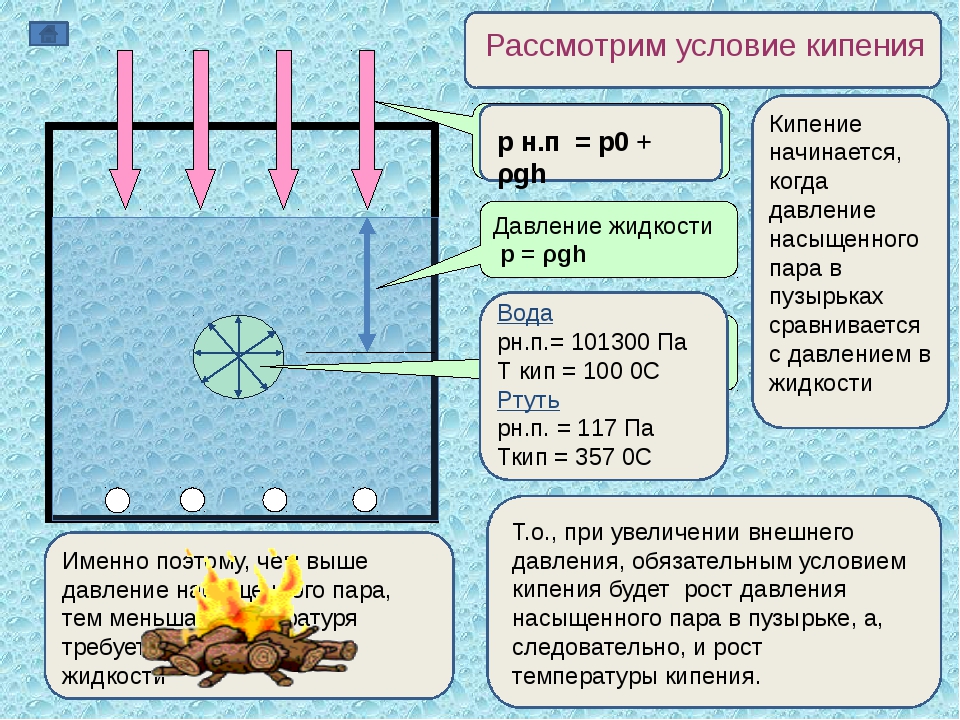
| Температура (градусы Цельсия) | Давление газа (МПа) |
|---|---|
| 0,01 | 0,000 612 |
| 25 | 0,003 17 |
| 50 | 0,012 35 |
| 75 | 0,0386 |
| 100 | 0,1014 |
| 150 | 0,4762 |
| 200 | 1,555 |
| 250 | 3.976 |
| 300 | 8,588 |
| 350 | 16,529 |
| 373,946 | 22,064 |
Первое значение в таблице соответствует тройной точке воды,
которое является термодинамическим состоянием, когда пар, жидкость и
твердые сосуществуют. Последнее значение соответствует критической точке воды.
Критическая точка — это конец кривой давления пара;
там паровая и жидкая фазы становятся идентичными и при
при более высоких температурах наблюдается только одна жидкая фаза.
Обновлено 26 апреля 2000 г.
Как вскипятить воду, температура кипения воды, Whats Cooking America
Температура кипения воды
Уровни моря в зависимости от температуры воды на больших высотах
Как вскипятить воду:
Кипячение воды очень легко сделать, но она очень важна для многих блюд, таких как приготовление риса и макаронных изделий.
Выберите кастрюлю, достаточно большую, чтобы вместить столько воды, которое вы хотите вскипятить, и подходящую крышку.
У вас может возникнуть соблазн использовать уже теплую или горячую воду из-под крана, но эта вода уже некоторое время находится в ваших трубах и становится несвежей. Используйте холодную воду, если собираетесь ее пить или готовить.
Не заполняйте кастрюлю полностью. Имейте в виду, что все, что вы добавляете в кипящую воду, увеличивает объем, и, кроме того, вам нужно будет оставить место для этих пузырьков, чтобы они могли делать свое дело. Например, если в кастрюле недостаточно места, рис или макароны выкипят.
Например, если в кастрюле недостаточно места, рис или макароны выкипят.
Поставьте кастрюлю на плиту и включите сильный огонь. Если хотите ускорить процесс, наденьте на него крышку
Проверьте, выходит ли пар из-под крышки, затем осторожно поднимите крышку, чтобы посмотреть, как течет вода.
Посмотрите на воду. Если со дна горшка на поверхность поднимаются большие пузыри, вода кипит. ПРИМЕЧАНИЕ. Маленькие пузырьки, которые остаются на дне или по бокам кастрюли, представляют собой пузырьки воздуха, присутствующие в воде; они не обязательно указывают на неизбежность закипания.Подождите, пока пузырьки поднимутся на верхнюю часть горшка.
Большая высота:
Вода закипает на большой высоте, но она не такая горячая, как кипящая вода на уровне моря. Это связано с тем, что на большой высоте давление воздуха ниже. Кипение происходит, когда вода достаточно горячая, чтобы иметь такое же давление, что и окружающий воздух, поэтому в ней могут образовываться пузырьки. На больших высотах давление воздуха ниже, чем на уровне моря, поэтому вода не должна сильно нагреваться, чтобы закипеть.
На больших высотах давление воздуха ниже, чем на уровне моря, поэтому вода не должна сильно нагреваться, чтобы закипеть.
Поскольку температура кипящей воды на больших высотах ниже, чем на уровне моря, приготовление пищи на больших высотах занимает больше времени, чем на уровне моря. Скорость приготовления пищи не зависит от времени, необходимого для кипячения.
Если добавить в воду немного соли, вода закипит при немного более высокой температуре, что может быть полезно при приготовлении пищи, особенно на большой высоте.
Температура кипения воды:
Из книги Kitchen Science Ховарда Хиллмана
.
Соль: Соль, сахар и практически любые другие вещества повышают температуру кипения и, следовательно, сокращают время приготовления.Разница в температуре между несоленой и соленой водой (одна чайная ложка соли на литр воды) составляет от 1 до 2 градусов по Фаренгейту, разница, которая может иметь решающее значение в ситуациях приготовления, требующих точности.
Жесткая вода: Жесткая вода означает воду с высоким уровнем растворенных минеральных солей. Поэтому жесткая вода закипает при более высокой температуре. Разница в температуре кипения между типичными поставками жесткой и мягкой воды составляет примерно один-два градуса.
Спирт: Спирт имеет более низкую температуру кипения, чем вода (около 175 градусов по Фаренгейту).по сравнению с 212 градусами по Фаренгейту). Если разбавить воду спиртом, смесь будет иметь более низкую температуру кипения, пока спирт полностью не испарится. Если вы решите изменить существующий рецепт, заменив часть воды изрядной долей вина, не забудьте увеличить время приготовления на 5-10 процентов в зависимости от крепости вина и тяжести вашего прикосновения.
Погода: Температура кипения воды на градус или два ниже в штормовые, а не ясные дни.Следовательно, вареная пища в ненастный день будет готовиться дольше.
Кастрюли разного размера : Будет ли вода закипать при более высокой температуре в высокой и узкой кастрюле, чем в короткой и широкой? Да. Поскольку высокий узкий горшок имеет большую глубину, вода, лежащая на дне, находится под большим давлением воды над ним, чем вода на дне короткого и широкого горшка. Чем больше давление, тем выше температура кипения. Разница составляет примерно 1 градус F.
Поскольку высокий узкий горшок имеет большую глубину, вода, лежащая на дне, находится под большим давлением воды над ним, чем вода на дне короткого и широкого горшка. Чем больше давление, тем выше температура кипения. Разница составляет примерно 1 градус F.
Высота: Чем выше высота, тем ниже атмосферное давление. Чем меньше атмосферное давление оказывает давление на поверхность жидкости, тем легче молекулам воды вылетать в воздух. Таким образом, в городе Денвер высотой в милю вода быстро закипает при более низкой температуре, чем в прибрежном Майами. На каждую тысячу футов над уровнем моря температура кипения воды падает почти на 2 градуса F.
Температура воды:
Приблизительные температуры кипения воды
Высота — температура
Уровень моря — 212 градусов F.- 100 градусов С.
1000 футов — 210,2 ° F — 99,00 ° C
2000 футов — 208,5 градусов по Фаренгейту — 98,06 градусов Цельсия
3000 футов — 206,7 градусов по Фаренгейту — 97,06 градусов по Цельсию
5000 футов — 203,2 ° F — 95,11 ° C
7500 футов — 198,9 градусов по Фаренгейту — 92,72 градусов по Цельсию
10 000 футов — 194,7 ° F -90,39 ° C
15000 футов -185,0 градусов по Фаренгейту — 85,00 градусов по Цельсию
Большая высота: Вода закипает при температуре ниже 212 градусов по Фаренгейту. (приблизительно 96 градусов по Фаренгейту). Каждое увеличение высоты на 500 футов вызывает падение температуры кипения примерно на 1 градус.
(приблизительно 96 градусов по Фаренгейту). Каждое увеличение высоты на 500 футов вызывает падение температуры кипения примерно на 1 градус.
Уровень моря: Вода кипит при 212 ° F и кипит при 190 ° F
Теплая вода — от 85 до 105 градусов по Фаренгейту. Температура воды сопоставима с температурой человеческого тела.
Теплая вода — от 115 до 120 градусов по Фаренгейту — Вода ощутима, но не горячая.
Горячая вода — от 130 до 135 градусов по Фаренгейту — вода слишком горячая, чтобы не повредить ее.
Poach — от 160 до 180 градусов F. — Вода начинает двигаться, дрожать.
Варить на медленном огне — от 185 до 200 градусов по Фаренгейту — Есть движение, и в воде появляются маленькие пузырьки.
Медленное кипение — 205 градусов по Фаренгейту — Движение больше, пузыри заметно больше.
Real Boil — 212 градусов по Фаренгейту — вода бурлит, бурно пузырится и дымится.
Дополнительные интересные статьи о воде:
Вода — Фонтан молодости — Я уверен, что вы слышали это много раз: «Пейте больше воды, это полезно для вас!» Тысячи лет люди всех стран искали мифический фонтан молодости. Если бы я сказал вам, что есть что-то, что придаст вам красивой сияющей кожи, уменьшит эти тонкие линии и морщины, повысит ваш уровень энергии и поможет вашему здоровью в целом, я уверен, вы бы послушали и заинтересуются. Все время этот фонтан молодости был здесь, в нашей повседневной жизни. Да, источник молодости — вода!
Если бы я сказал вам, что есть что-то, что придаст вам красивой сияющей кожи, уменьшит эти тонкие линии и морщины, повысит ваш уровень энергии и поможет вашему здоровью в целом, я уверен, вы бы послушали и заинтересуются. Все время этот фонтан молодости был здесь, в нашей повседневной жизни. Да, источник молодости — вода!
Браконьерство против кипячения и кипячения. Разница между варкой, варкой и варкой — это всего лишь вопрос температуры.
Миф о точке кипения
Хасок Чанг
Кафедра истории и философии науки
Кембриджский университет
18 октября 2007 г.
Об авторе / Связаться с автором
В школе мы все узнаем, что чистая вода всегда кипит при 100 ° C (212 ° F) при нормальном атмосферном давлении.Как и многие другие вещи, которые «знают все», это миф. Мы должны прекратить увековечивать этот миф в школах и университетах, а также в повседневной жизни: он не только неверен, но и передает ложные представления о природе научного знания. И в отличие от некоторых других мифов, он не выполняет достаточно полезных функций.
И в отличие от некоторых других мифов, он не выполняет достаточно полезных функций.
На самом деле существует множество вариаций температуры кипения воды. Например, разница в несколько градусов зависит от материала емкости, в которой происходит кипячение.Удаление растворенного воздуха из воды может легко повысить ее температуру кипения примерно на 10 градусов по Цельсию.
Неустойчивость точки кипения — это то, что когда-то было широко известно среди ученых. Это довольно легко проверить, как я узнал из простых экспериментов, которые я показываю в этой статье. И это до сих пор известно некоторым сегодняшним экспертам. Итак, на самом деле странная вещь: почему мы все не слышим об этом? Не только это, но и почему большинство из нас верят в противоположность тому, что есть на самом деле, и поддерживают это с такой уверенностью? Как явная ложь стала научным здравым смыслом?
Впервые я осознал всю эту проблему несколько лет назад, когда работал над моей недавней книгой Inventing Temperature (New York: Oxford University Press, 2004), историческим и философским трактатом о термометрах и концепции температуры ( прочтите Введение и оглавление книги).
Старый термометр, фото которого я поместил на обложку книги, говорит о многом (щелкните изображение, чтобы увеличить его). Этот инструмент, датируемый 1750-ми годами, хранится в Музее науки в Лондоне; стеклянные стержни отломились, поэтому все, что у нас есть, — это рамка, на которой изображены четыре разных шкалы. Третья — знакомая шкала Фаренгейта. (Второй, из-за Делиля, «перевернут», с 0 ° в точке кипения и увеличивающимися числами по мере того, как становится холоднее; подробнее о таких шкалах читайте на стр.160-162 дюйма Температура изобретения .)
На термометре отмечены две точки кипения. При знакомой температуре 212 ° F он говорит «яростно водяные мальчишки». При температуре около 204 ° F он говорит, что «закипает». Что здесь происходит?
Вы можете подумать, что ремесленник, который сделал этот термометр, вероятно, был довольно некомпетентен в научных вопросах. Но оказывается, что этот термометр был работой Джорджа Адамса, официального создателя научных приборов короля Георга III. А идея двух точек кипения на самом деле пришла прямо от Исаака Ньютона, чья температурная шкала, опубликованная в 1701 году, действительно была первой из четырех шкал Адамса.
А идея двух точек кипения на самом деле пришла прямо от Исаака Ньютона, чья температурная шкала, опубликованная в 1701 году, действительно была первой из четырех шкал Адамса.
Вернуться к началу
Вдохновленный этими странностями 18 века, я более глубоко заглянул в историю, чтобы увидеть, что люди действительно знали и думали о точке кипения в те ранние дни. Фактически, это было настолько неопределенным, что в 1776 году Лондонское королевское общество назначило специальный комитет, которому было поручено дать определенные рекомендации относительно «фиксированных точек» термометров.Комитет Королевского общества зафиксировал различные типы колебаний температуры кипения воды. Генри Кавендиш (портрет справа), возглавлявший комитет, оставил нам довольно загадочное заявление в одной из своих неопубликованных рукописей: «Превышение температуры воды выше точки кипения вызвано множеством разнообразных обстоятельств». (Подробнее о выводах Комитета Королевского общества. )
)
Еще одним ключевым членом комитета был Жан-Андре де Люк (слева), женевский геолог, физик, метеоролог, теолог и бизнесмен.К этому времени он жил в Англии, став «Читателем» королевы Шарлотты в Виндзоре. Около 1770 года Де Люк провел обширные исследования кипения. Он рассудил, что при обычном кипении слой воды, касающийся нагретой поверхности, где образуются пузырьки пара, должен быть намного горячее, чем остальная вода. Он хотел узнать температуру того «первого слоя», который будет температурой «истинного кипения». Поэтому он взял колбу с узким горлышком и нагрел ее на масляной ванне (а не на открытом огне), пытаясь довести всю воду до той же температуры путем медленного нагрева с минимальными потерями тепла на открытой поверхности. .Но когда он это сделал, Де Люк обнаружил, что вода вообще не кипит нормально. Пузыри были нечастыми и очень большими, иногда взрывоопасными; температура была высокой и неустойчивой, иногда доходившей до 103 ° C.
Де Люка ждала еще одна загадка. Он заметил, что присутствие растворенного воздуха в воде вызывает преждевременное кипение. Он пытался выпустить воздух различными способами, но в конце концов решил, что ему нужно долго встряхивать запечатанную бутылку с водой, помимо всего прочего (помните, как при стряхивании бутылки с газированным напитком выделяются пузырьки газа) .Он сообщил: «Эта операция длилась четыре недели, в течение которых я почти никогда не ставил фляжку, кроме как спать, делать дела в городе и делать то, что требовало обеих рук. Я ел, я читал, я писал, я видел друзья мои, я гулял, все время качая водой «. Четыре безумных недели тряски принесли свои плоды. Драгоценная безвоздушная вода Де Люка достигла 112,2 ° C, а затем взорвалась. (Подробнее о работе Де Люка по кипячению.)
Он заметил, что присутствие растворенного воздуха в воде вызывает преждевременное кипение. Он пытался выпустить воздух различными способами, но в конце концов решил, что ему нужно долго встряхивать запечатанную бутылку с водой, помимо всего прочего (помните, как при стряхивании бутылки с газированным напитком выделяются пузырьки газа) .Он сообщил: «Эта операция длилась четыре недели, в течение которых я почти никогда не ставил фляжку, кроме как спать, делать дела в городе и делать то, что требовало обеих рук. Я ел, я читал, я писал, я видел друзья мои, я гулял, все время качая водой «. Четыре безумных недели тряски принесли свои плоды. Драгоценная безвоздушная вода Де Люка достигла 112,2 ° C, а затем взорвалась. (Подробнее о работе Де Люка по кипячению.)
В течение XIX века дальнейшие исследования показали, что кипение является даже более сложным и непослушным явлением, чем предполагал Де Люк.Например, в 1810-х годах Жозеф-Луи Гей-Люссак из Парижа сообщил, что вода кипит при 101,2 ° C в стеклянном сосуде, тогда как в металлическом сосуде она кипит ровно при 100 ° C. Этот результат стал довольно хорошо известен, но в течение долгого времени ему не было окончательного объяснения. В 1842 году Франсуа Марсе в Женеве расширил работу Гей-Люссака и сообщил, что вода может достигать температуры выше 105 ° C в стеклянном сосуде, обработанном горячей серной кислотой. Это положило начало целому ряду исследований, в которых разные исследователи соревновались друг с другом в достижении все более и более высоких температур чистой жидкой воды при нормальном атмосферном давлении.Насколько я могу судить, в этой гонке «перегрев» выиграл немец по имени Георг Кребс, который в 1869 году достиг примерно 200 ° C. (Подробнее о работе 19-го века по перегреву).
Этот результат стал довольно хорошо известен, но в течение долгого времени ему не было окончательного объяснения. В 1842 году Франсуа Марсе в Женеве расширил работу Гей-Люссака и сообщил, что вода может достигать температуры выше 105 ° C в стеклянном сосуде, обработанном горячей серной кислотой. Это положило начало целому ряду исследований, в которых разные исследователи соревновались друг с другом в достижении все более и более высоких температур чистой жидкой воды при нормальном атмосферном давлении.Насколько я могу судить, в этой гонке «перегрев» выиграл немец по имени Георг Кребс, который в 1869 году достиг примерно 200 ° C. (Подробнее о работе 19-го века по перегреву).
Вернуться к началу
Я был очень удивлен, узнав об этом. Я думал, что у меня довольно хорошее научное образование, но я ни разу не слышал о таких вещах, когда изучал физику в бакалавриате — или в моей последующей жизни в качестве философа и историка науки, в которой я постоянно контактировал с коллеги, постоянно исследующие странные вещи, незавершенные дела и нерешенные вопросы в науке.
Я подробно изложил исторические дебаты в первой главе моей книги, упомянутой ранее, но у меня все еще оставалась проблема недоверия. Были ли правы ученые XVIII и XIX веков? Или это была ошибка, похожая на печально известный недавний случай «холодного синтеза» или более старый случай «N-лучей»? Я решил, что есть только один способ узнать это: увидеть сам, в лаборатории.
Мне удалось воплотить эту мысль в жизнь летом 2004 года, а затем снова в 2007 году благодаря гостеприимству коллег с химического факультета Лондонского университетского колледжа и исследовательскому гранту Leverhulme Trust.Мои эксперименты были достаточно простыми, но они не могли быть выполнены без щедрой помощи множества людей.
Я хотел бы представить шесть наборов экспериментов, очень кратко резюмированных ниже. Щелкните ссылки в конце каждой сводки, чтобы получить полное описание и видеоматериалы с основными моментами, а также некоторые дальнейшие заметки о других связанных экспериментах и наблюдениях.
Общие сведения об экспериментах и использованной аппаратуре .
Эксперимент 1.Неопределенность точки кипения
Почти как только я вошел в лабораторию, я понял, что обычное кипение — очень сложное и довольно неопределенное явление, о чем свидетельствует термометр Адамса, о котором говорилось выше.
Прочтите об этом эксперименте и посмотрите видеоклип.
Подробнее о связанных экспериментах и наблюдениях.
Эксперимент 2. Различная температура в разных сосудах
После наблюдения за очень обычным кипением воды с некоторой осторожностью, следующим очевидным шагом было проверить утверждение Гей-Люссака о том, что на температуру кипения влияет материал сосуда, в котором происходило кипение.В моих экспериментах легко наблюдались различия в диапазоне более 3 ° C — самые низкие для металла, более высокие для стекла и самые высокие в некоторых керамических сосудах.
Прочтите об этом эксперименте и посмотрите видеоклип.
Подробнее о связанных экспериментах и наблюдениях.
Эксперимент 3. Пониженная температура в гидрофобном сосуде
Эти наблюдения привели к дальнейшим экспериментам. Гей-Люссак объяснил влияние качества поверхности тем, что температура кипения была выше, когда вода сильнее прилипала к поверхности сосуда.Когда Марсе развил работу Гей-Люссака, он заметил, что стеклянный стакан, покрытый слоем серы, которая отталкивает воду, показывает температуру кипения 99,7 ° C. Услышав это, мой спонсор-химик Андреа Селла посоветовал нам попробовать современную версию эксперимента, которая, конечно же, дает значительно более низкие температуры кипения. (Примечание для историков: разве нет опасений по поводу использования тех же материалов, что и историки?)
Прочтите об этом эксперименте и посмотрите видеоклип.
Опыт 4. Действие кипящей щепы
Гей-Люссак также сообщил, что бросание металлических опилок или даже порошкового стекла в кипящую воду в стеклянном сосуде снижает температуру, приближая ее к 100 ° C. Фактически, эта идея позже была развита до использования «кипящих чипсов», чтобы избежать перегрева и облегчить плавное кипение, что является обычной практикой в химических лабораториях и по сей день. Кипячение чипсов позволяет воде закипать при значительно более низких температурах.
Фактически, эта идея позже была развита до использования «кипящих чипсов», чтобы избежать перегрева и облегчить плавное кипение, что является обычной практикой в химических лабораториях и по сей день. Кипячение чипсов позволяет воде закипать при значительно более низких температурах.
Прочтите об этом эксперименте и посмотрите видеоклип.
Подробнее о связанных экспериментах и наблюдениях.
( Примечание по безопасности и оборудованию : Эксперименты 1-4 действительно очень просты, требуют минимальных материалов и навыков, хотя может быть нетривиальной задачей получить запас дистиллированной воды, если вы не работаете в установленной лаборатории. Следующее два эксперимента немного сложнее, и их, конечно, не следует проводить без защиты глаз, так как из колб будет выходить очень горячая вода.)
Эксперимент 5. Перегретое кипение при медленном нагревании
Я провел длинную серию экспериментов, пытаясь повторить работу Де Люка, опубликованную в 1772 году, чтобы изучить, что происходит, когда воду кипятят с использованием мягкого источника тепла, минимизируя потери тепла на поверхности. В этой установке кипение обычно начинается при температуре около 100 ° C, но постепенно вода начинает «вздыматься» и «вздуваться». Температура может легко достигать 103-104 ° C.
В этой установке кипение обычно начинается при температуре около 100 ° C, но постепенно вода начинает «вздыматься» и «вздуваться». Температура может легко достигать 103-104 ° C.
Прочтите об этом эксперименте и посмотрите видеоклип.
Подробнее о связанных экспериментах и наблюдениях.
Эксперимент 6. Перегрев за счет дегазации
Наконец, я попытался воспроизвести результат Де Люка по удалению растворенного воздуха из воды. Но, в отличие от Де Люка, я не хотел трястись четырьмя неделями, поэтому я нашел альтернативный метод. (Узнайте больше о процессе «дегазации».) Когда дегазированная вода мягко нагревается, результат часто бывает весьма замечательным: в течение долгого времени ничего видимого не происходит, а затем внезапно вода взрывается.Я наблюдал, как непосредственно перед взрывом температура достигала 108-109 ° C. Кто-нибудь еще видел это?
Прочтите об этом эксперименте и посмотрите видеоклип.
Подробнее о связанных экспериментах и наблюдениях.
Вернуться к началу
Надеюсь, из моих экспериментов вы легко увидите, что странные наблюдения, о которых сообщали ученые 18 и 19 веков, в целом были вполне правильными. Это поднимает несколько очень интересных вопросов.
(1) Если точка кипения настолько неопределенная, как можно сделать стандартные термометры? Великая ирония: результат, что вода не всегда кипит при 100 ° C, был установлен с помощью термометров, которые были откалиброваны в предположении, что кипит при 100 ° C. Эта кажущаяся чушь на самом деле не так плоха, как кажется. Читать далее.
(2) Если температура кипящей воды так непостоянна при вполне обыденных обстоятельствах, почему мы не замечаем этого, когда большинство из нас кипятят воду ежедневно? Это только потому, что большинство людей до сих пор кипятят воду в тех условиях, которые преобладали в Европе 19 века. Я защищаю безумный культурный релятивизм? Читать далее.
Я защищаю безумный культурный релятивизм? Читать далее.
(3) Почему ученые не придумали теорию, объясняющую эти странные явления? На самом деле, такая теория существует, и есть хорошо зарекомендовавшая себя экспериментальная работа, связанная с теорией — не столько в физике или химии, сколько в инженерии. (Впервые я узнал об этом в разгар своих экспериментов благодаря Стиву Брамвеллу и Майку Юингу из химического факультета Калифорнийского университета в Лос-Анджелесе.) Подробнее.
Вернуться к началу
Мое расследование вызвало гораздо больше вопросов, чем дало ответов.Есть вещи, которые мне еще не удалось понять, например, как именно и почему растворенный воздух играет такую важную роль в облегчении кипения. (Подробнее об оставшихся вопросах и дальнейшей работе.) Но уже мое предварительное исследование выявило некоторые существенные пробелы в общих знаниях о кипении в стандартной физике и химии, особенно в том, как преподаются эти предметы, даже в высших учебных заведениях. Эти пробелы существуют не потому, что наука неспособна их заполнить, а потому, что науке нужно отложить в сторону множество вопросов и фактов, чтобы сосредоточиться на текущих передовых исследованиях.
Эти пробелы существуют не потому, что наука неспособна их заполнить, а потому, что науке нужно отложить в сторону множество вопросов и фактов, чтобы сосредоточиться на текущих передовых исследованиях.
История и философия науки могут служить функции сохранения и развития аспектов научного знания, которые утрачиваются или игнорируются в процессе научного прогресса. Я бы никогда не узнал всех хороших вещей о кипячении, которые я представил в этой статье, если бы я не узнал из исторических источников. И я бы не стал изучать эту историю, если бы не исследовал философские вопросы о том, как мы можем узнать, надежны ли наши термометры.
Использование истории и философии науки для улучшения наших знаний о природе — это программа исследования, которую я называю «дополнительной наукой», потому что она дополняет текущую специализированную науку, не оспаривая ее законность (подробнее о дополнительной науке). Я надеюсь, что это краткое изложение конкретного вопроса дало вам представление о потенциале этой исследовательской программы, которой я планирую заниматься в течение многих лет.
Вернуться к началу
Точка кипения воды vs.Высота
Температура кипения воды уменьшается с высотой:
| Высота — по сравнению с уровнем моря | Точка кипения | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| (фут) | (м) | ( o F) | ( o C) | |||||||||
| -1000 | -305 | 213,9 | 101,1 | |||||||||
| -750 | -229 | 213.5 | 100,8 | |||||||||
| -500 | -152 | 213,0 | 100,5 | |||||||||
| -250 | -76 | 212,5 | 100,3 | |||||||||
| 0 | 0 | 212,0 | 100,0 | |||||||||
| 250 | 76 | 211,5 | 99,7 | |||||||||
| 500 | 152 | 211,0 | 99,5 | |||||||||
| 750 | 229 | 210. 5 5 | 99,2 | |||||||||
| 1000 | 305 | 210,1 | 98,9 | |||||||||
| 1250 | 381 | 209,6 | 98,6 | |||||||||
| 1500 | 457 | 209,1 | 98,4 | 533 | 208,6 | 98,1 | ||||||
| 2000 | 610 | 208,1 | 97,8 | |||||||||
| 2250 | 686 | 207.6 | 97,6 | |||||||||
| 2500 | 762 | 207,2 | 97,3 | |||||||||
| 2750 | 838 | 206,7 | 97,1 | |||||||||
| 3000 | 914 | 206,2 | 96,8 | 991 | 205,7 | 96,5 | ||||||
| 3500 | 1067 | 205,3 | 96,3 | |||||||||
| 3750 | 1143 | 204.8 | 96,0 | |||||||||
| 4000 | 1219 | 204,3 | 95,7 | |||||||||
| 4250 | 1295 | 203,8 | 95,5 | |||||||||
| 4500 | 1372 | 203,4 | 95,2 | |||||||||
| 1448 | 202,9 | 94,9 | ||||||||||
| 5000 | 1524 | 202,4 | 94,7 | |||||||||
| 5250 | 1600 | 202. 0 0 | 94,4 | |||||||||
| 5500 | 1676 | 201,5 | 94,2 | |||||||||
| 5750 | 1753 | 201,0 | 93,9 | |||||||||
| 6000 | 1829 | 200,6 | 93,6 | 1905 | 200,1 | 93,4 | ||||||
| 6500 | 1981 | 199,6 | 93,1 | |||||||||
| 6750 | 2057 | 199.2 | 92,9 | |||||||||
| 7000 | 2134 | 198,7 | 92,6 | |||||||||
| 7250 | 2210 | 198,2 | 92,4 | |||||||||
| 7500 | 2286 | 197,8 | 92,1 | 2362 | 197,3 | 91,8 | ||||||
| 8000 | 2438 | 196,9 | 91,6 | |||||||||
| 8250 | 2515 | 196.4 | 91,3 | |||||||||
| 8500 | 2591 | 196,0 | 91,1 | |||||||||
| 8750 | 2667 | 195,5 | 90,8 | |||||||||
| 9000 | 2743 | 195,0 | 90,627 | 2819 | 194,6 | 90,3 | ||||||
| 9500 | 2896 | 194,1 | 90,1 | |||||||||
| 9750 | 2972 | 193.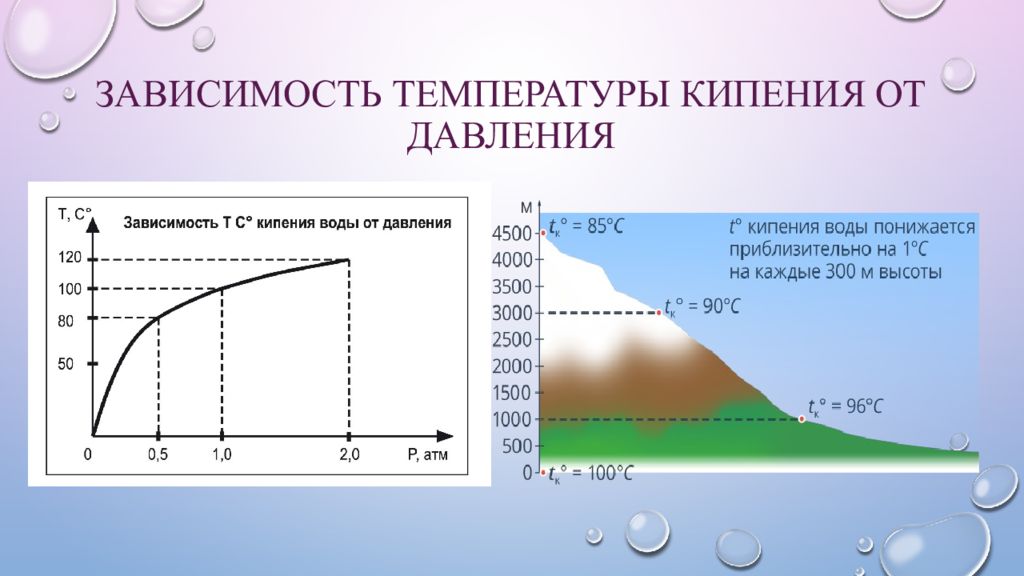 7 7 | 89,8 | |||||||||
| 10000 | 3048 | 193,2 | 89,6 | |||||||||
| 10250 | 3124 | 192,8 | 89,3 | |||||||||
| 10500 | 3200 | 192,3 | 89,1 | 3277 | 191,9 | 88,8 | ||||||
| 11000 | 3353 | 191,4 | 88,6 | |||||||||
| 11250 | 3429 | 191.0 | 88,3 | |||||||||
| 11500 | 3505 | 190,5 | 88,1 | |||||||||
| 11750 | 3581 | 190,1 | 87,8 | |||||||||
| 12000 | 3658 | 189,7 | 87,627 | 3734 | 189,2 | 87,3 | ||||||
| 12500 | 3810 | 188,8 | 87,1 | |||||||||
| 12750 | 3886 | 188.3 | 86,8 | |||||||||
| 13000 | 3962 | 187,9 | 86,6 | |||||||||
| 13250 | 4037 | 187,4 | 86,4 | |||||||||
| 13500 | 4115 | 187,0 | 86,1 13750 | 4191 | 186,6 | 85,9 | ||||||
| 14000 | 4267 | 186,1 | 85,6 | |||||||||
| 14250 | 4343 | 185.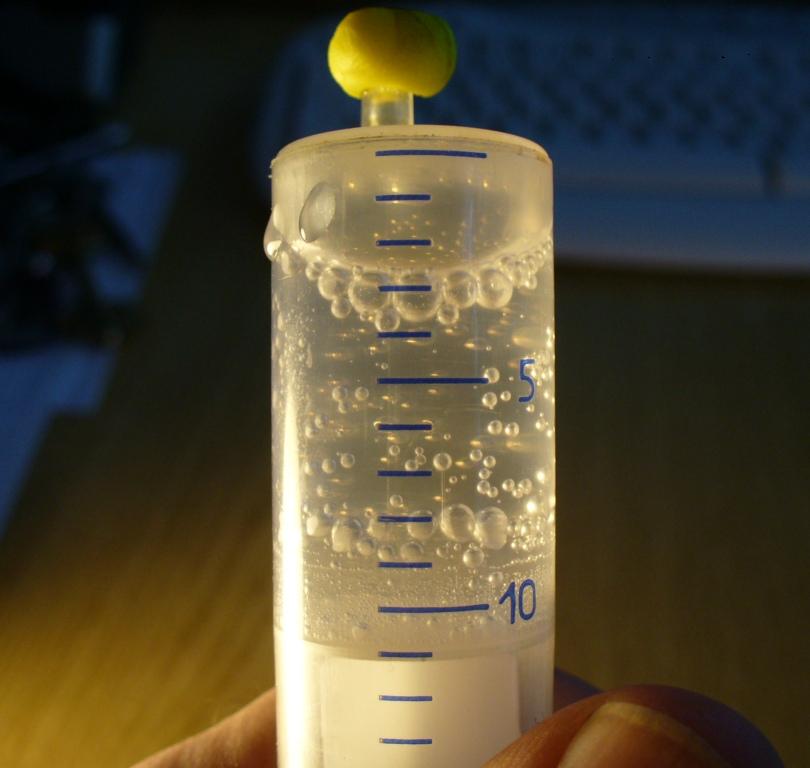 7 7 | 85,4 | |||||||||
| 14500 | 4420 | 185,3 | 85,1 | |||||||||
| 14750 | 4496 | 184,8 | 84,9 | |||||||||
| 15000 | 4572 | 184,4 | 84,7 | 4648 | 184,0 | 84,4 | ||||||
| 15500 | 4724 | 183,5 | 84,2 | |||||||||
| 15750 | 4801 | 183.1 | 83,9 | |||||||||
| 16000 | 4877 | 182,7 | 83,7 | |||||||||
| 16250 | 4953 | 182,2 | 83,5 | |||||||||
| 16500 | 5029 | 181,8 | 83,2 16750 | 5105 | 181,4 | 83,0 | ||||||
| 17000 | 5182 | 180,9 | 82,7 | |||||||||
| 17250 | 5258 | 180.5 | 82,5 | |||||||||
| 17500 | 5334 | 180,1 | 82,3 | |||||||||
| 17750 | 5410 | 179,7 | 82,0 | |||||||||
| 18000 | 5486 | 179,2 | 81,88 | 5563 | 178,8 | 81,6 | ||||||
| 18500 | 5639 | 178,4 | 81,3 | |||||||||
| 18750 | 5715 | 178.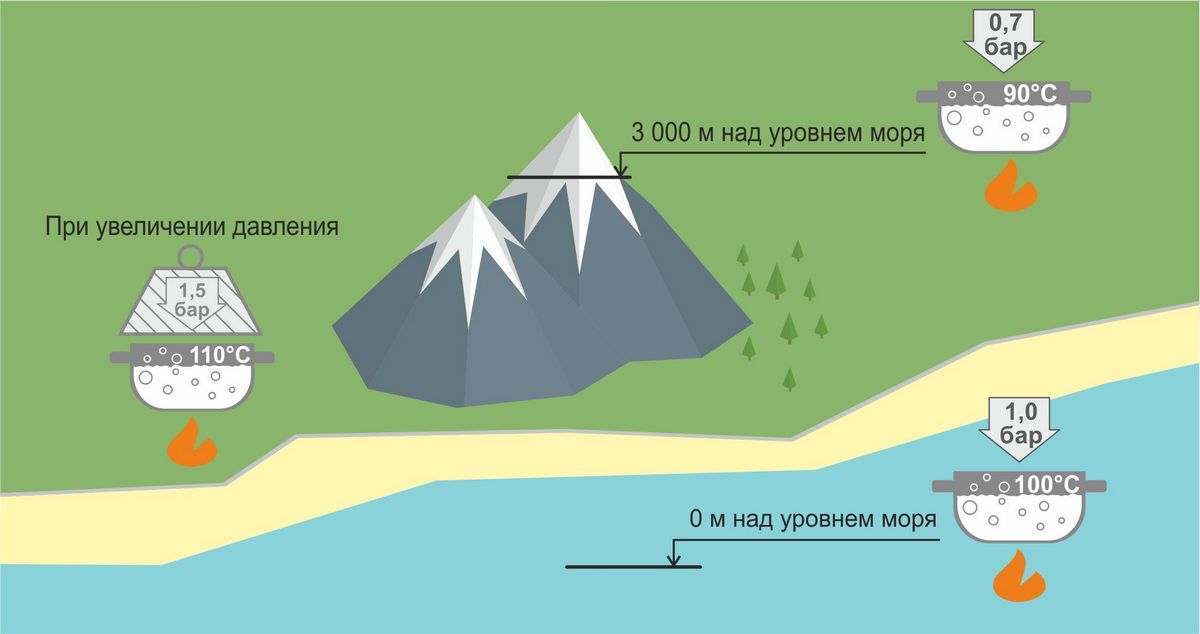 0 0 | 81,1 | |||||||||
| 19000 | 5791 | 177,6 | 80,9 | |||||||||
| 19250 | 5867 | 177,1 | 80,6 | |||||||||
| 19500 | 5944 | 176,7 | 80,427 | |||||||||
| 6020 | 176,3 | 80,2 | ||||||||||
| 20000 | 6096 | 175,9 | 79,9 | |||||||||
| 20250 | 6172 | 175.5 | 79,7 | |||||||||
| 20500 | 6248 | 175,1 | 79,5 | |||||||||
| 20750 | 6325 | 174,7 | 79,3 | |||||||||
| 21000 | 6401 | 174,2 | 6401 | 174,2 | 21250 | 6477 | 173,8 | 78,8 | ||||
| 21500 | 6553 | 173,4 | 78,6 | |||||||||
| 21750 | 6629 | 173.0 | 78,3 | |||||||||
| 22000 | 6706 | 172,6 | 78,1 | |||||||||
| 22250 | 6782 | 172,2 | 77,9 | |||||||||
| 22500 | 6858 | 171,8 | 22750 | 6934 | 171,4 | 77,4 | ||||||
| 23000 | 7010 | 171,0 | 77,2 | |||||||||
| 23250 | 7087 | 170. 6 6 | 77,0 | |||||||||
| 23500 | 7163 | 170,2 | 76,8 | |||||||||
| 23750 | 7239 | 169,8 | 76,5 | |||||||||
| 24000 | 7315 | 169,4 | 7315 | 169,4 | 24250 | 7391 | 169,0 | 76,1 | ||||
| 24500 | 7468 | 168,6 | 75,9 | |||||||||
| 24750 | 7544 | 168.2 | 75,6 | |||||||||
| 25000 | 7620 | 167,8 | 75,4 | |||||||||
| 25250 | 7696 | 167,4 | 75,2 | |||||||||
| 25500 | 7772 | 167,0 | 75772 | 167,0 | 25750 | 7849 | 166,6 | 74,8 | ||||
| 26000 | 7925 | 166,2 | 74,5 | |||||||||
| 26250 | 8001 | 165.8 | 74,3 | |||||||||
| 26500 | 8077 | 165,4 | 74,1 | |||||||||
| 26750 | 8153 | 165,0 | 73,9 | |||||||||
| 27000 | 8230 | 164,6 | 73,7 | 8306 | 164,2 | 73,5 | ||||||
| 27500 | 8382 | 163,8 | 73,2 | |||||||||
| 27750 | 8458 | 163. 4 4 | 73,0 | |||||||||
| 28000 | 8534 | 163,1 | 72,8 | |||||||||
| 28250 | 8611 | 162,7 | 72,6 | |||||||||
| 28500 | 8687 | 162,3 | 72,4 28750 | 8763 | 161,9 | 72,2 | ||||||
| 29000 | 8839 | 161,5 | 72,0 | |||||||||
| 29250 | 8916 | 161.1 | 71,7 | |||||||||
| 29500 | 8992 | 160,7 | 71,5 | |||||||||
| 29750 | 9068 | 160,4 | 71,3 | |||||||||
| 30000 | 9144 | 160,0 | 71,190 | |||||||||


 34
34 ru/vidy-vody/seawater/pochemu-nelzya-pit-morskuyu-vodu.html, это очень интересно!
ru/vidy-vody/seawater/pochemu-nelzya-pit-morskuyu-vodu.html, это очень интересно! 0
0 8
8 Но как часто вы на самом деле думаете о скрытых сложностях, связанных с тем, чтобы бросить горшок с водой на конфорку?
Но как часто вы на самом деле думаете о скрытых сложностях, связанных с тем, чтобы бросить горшок с водой на конфорку?
 Но что может повлиять на эту температуру и что все это значит для вашей готовки?
Но что может повлиять на эту температуру и что все это значит для вашей готовки? Пузырьки с боков и со дна горшка начали подниматься на поверхность. Обычно вы видите несколько струйок крошечных пузырьков, похожих на шампанское, поднимающихся со дна кастрюли. Однако по большей части жидкость все еще относительно неподвижна. Это температурный диапазон, который вам нужен при приготовлении бульона или при медленном приготовлении нежных тушеных и тушеных блюд. Гораздо ниже, и их приготовление займет слишком много времени. Гораздо выше, и вы рискуете высушить мясо.
Пузырьки с боков и со дна горшка начали подниматься на поверхность. Обычно вы видите несколько струйок крошечных пузырьков, похожих на шампанское, поднимающихся со дна кастрюли. Однако по большей части жидкость все еще относительно неподвижна. Это температурный диапазон, который вам нужен при приготовлении бульона или при медленном приготовлении нежных тушеных и тушеных блюд. Гораздо ниже, и их приготовление займет слишком много времени. Гораздо выше, и вы рискуете высушить мясо. Д.
Д. Более низкая плотность означает более низкое атмосферное давление. Более низкое атмосферное давление означает, что молекулам воды требуется меньше энергии для выхода в воздух. Все это означает, что все, что происходит с нашей драгоценной водной шкалой на уровне моря, происходит при гораздо более низких температурах на больших высотах.
Более низкая плотность означает более низкое атмосферное давление. Более низкое атмосферное давление означает, что молекулам воды требуется меньше энергии для выхода в воздух. Все это означает, что все, что происходит с нашей драгоценной водной шкалой на уровне моря, происходит при гораздо более низких температурах на больших высотах.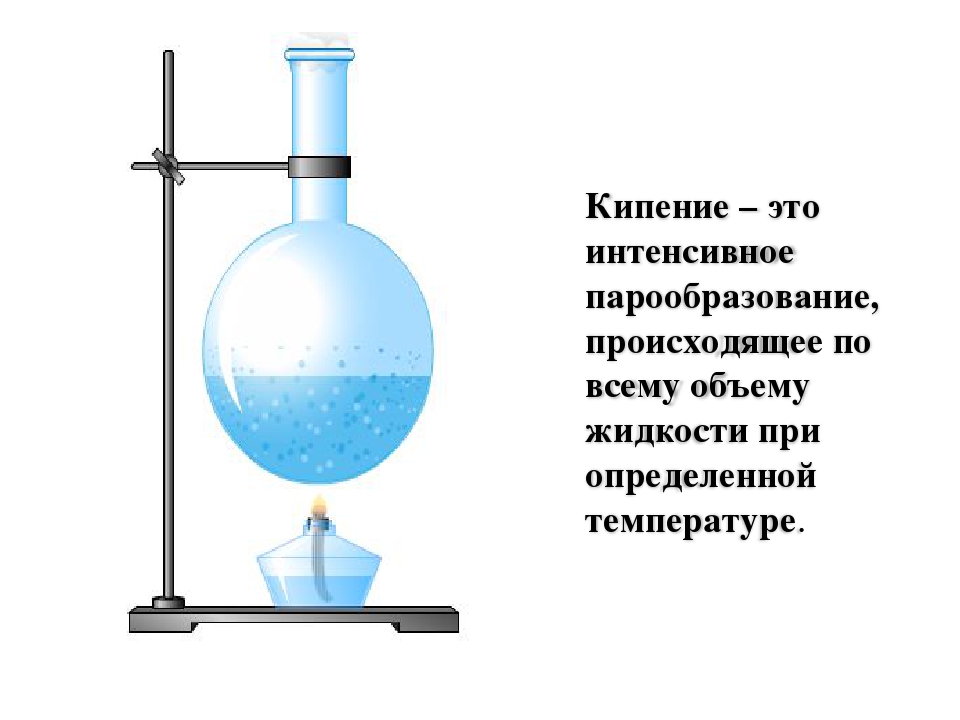 Поднимитесь достаточно высоко, и вы даже не сможете приготовить овощи, которые необходимо нагреть как минимум до 183 ° F, чтобы они распались.
Поднимитесь достаточно высоко, и вы даже не сможете приготовить овощи, которые необходимо нагреть как минимум до 183 ° F, чтобы они распались. Иногда лучшее, что вы можете сделать, — это похлопать своих склонных к возвышению друзей по спине и сказать: «Не повезло. Возможно, в следующий раз вы не будете так думать о себе в высшей степени ».
Иногда лучшее, что вы можете сделать, — это похлопать своих склонных к возвышению друзей по спине и сказать: «Не повезло. Возможно, в следующий раз вы не будете так думать о себе в высшей степени ». Кипящая или замерзающая вода удаляет растворенные газы (в основном кислород), что может незначительно повлиять на температуру кипения.Настолько незначительный, что ни мой таймер, ни градусник не могли обнаружить никакой разницы.
Кипящая или замерзающая вода удаляет растворенные газы (в основном кислород), что может незначительно повлиять на температуру кипения.Настолько незначительный, что ни мой таймер, ни градусник не могли обнаружить никакой разницы. Вода закипает при температуре 212 ° F, а спирт — при температуре около 173 ° F, так что наверняка спирт полностью испарится еще до того, как вы сделаете вмятину в воде, верно? Неа. Даже после трех часов кипячения в рагу останутся хорошие 5% алкоголя.Готовьте его с закрытой крышкой, и это число возрастает до десяти раз. Для большинства людей недостаточно выпивки, но трезвенник может иметь в виду кое-что.
Вода закипает при температуре 212 ° F, а спирт — при температуре около 173 ° F, так что наверняка спирт полностью испарится еще до того, как вы сделаете вмятину в воде, верно? Неа. Даже после трех часов кипячения в рагу останутся хорошие 5% алкоголя.Готовьте его с закрытой крышкой, и это число возрастает до десяти раз. Для большинства людей недостаточно выпивки, но трезвенник может иметь в виду кое-что. Горстка соли быстро вводит тысяч центров зародышеобразования, облегчая образование и выход пузырьков.
Горстка соли быстро вводит тысяч центров зародышеобразования, облегчая образование и выход пузырьков. обе формы электромагнитного излучения). Микроволны используют этот факт, испуская волны, которые заставляют молекулы воды быстро перемещаться вперед и назад. Это движение, в свою очередь, нагревает вашу пищу.
обе формы электромагнитного излучения). Микроволны используют этот факт, испуская волны, которые заставляют молекулы воды быстро перемещаться вперед и назад. Это движение, в свою очередь, нагревает вашу пищу. Этого не происходит на плите, поскольку нагревание снизу кастрюли создает множество конвекционных потоков (движение, которое происходит между относительно горячими и прохладными областями жидкости или газа).
Этого не происходит на плите, поскольку нагревание снизу кастрюли создает множество конвекционных потоков (движение, которое происходит между относительно горячими и прохладными областями жидкости или газа). Хорошие новости для вас, потому что это как раз в оптимальной температурной зоне тушения на глубине кипения.
Хорошие новости для вас, потому что это как раз в оптимальной температурной зоне тушения на глубине кипения.